हेलो स्टूडेंट्स, यहां हमने राजस्थान बोर्ड कक्षा 11वीं की रसायन विज्ञान सॉल्यूशंस को दिया हैं। यह solutions स्टूडेंट के परीक्षा में बहुत सहायक होंगे | Student RBSE solutions for Class 11 Chemistry Chapter 14 पर्यावरणीय रसायन pdf Download करे| RBSE solutions for Class 11 Chemistry Chapter 14 पर्यावरणीय रसायन notes will help you.
Table of Contents
Rajasthan Board RBSE Class 11 Chemistry Chapter 14 पर्यावरणीय रसायन
RBSE Class 11 Chemistry Chapter 14 पाठ्यपुस्तक के अभ्यास प्रश्न
RBSE Class 11 Chemistry Chapter 14 वस्तुनिष्ठ प्रश्न
प्रश्न 1.
PAN का अर्थ है?
(अ) परऑक्सी ऐल्डीहाइड नाइट्रेट
(ब) परऑक्सी अमोनियम नाइट्रेट
(स) परऑक्सी ऐसीटाइल नाइट्रेट
(द) कोई नहीं
प्रश्न 2.
कणीय वायु प्रदूषक है –
(अ) क्लोरीन
(ब) कोयला
(स) अमोनिया
(द) उपरोक्त सभी
प्रश्न 3.
वैश्विक तापन का प्रमुख कारण है –
(अ) अम्ल वर्षा
(ब) नाभिकीय दुर्घटनाएँ
(स) तेजी से गर्मी पड़ना
(द) हरित गृह प्रभाव
प्रश्न 4.
CFC’s का प्रयोग किया जाता है।
(अ) प्रशीतकों में
(ब) प्लास्टिक निर्माण में
(स) बिजली के उपकरणों में
(द) उपरोक्त सभी में
प्रश्न 5.
निम्नलिखित में से ग्रीन हाउस गैस नहीं है –
(अ) CO2
(ब) CH4
(स) COCl2
(द) N2O
प्रश्न 6.
ओजोन में ऑक्सीजन के परमाणुओं की संख्या होती है –
(अ) 3
(ब) 2
(स) 1
(द) 4
उत्तरमाला:
1. (स)
2. (ब)
3. (द)
4. (अ)
5. (स)
6. (अ)
RBSE Class 11 Chemistry Chapter 14 अतिलघूत्तरात्मक प्रश्न
प्रश्न 7.
ग्रीन हाउस प्रभाव से आप क्या समझते हैं?
उत्तर:
पृथ्वी के वातावरण में उपस्थित कार्बन डाइऑक्साइड, मेथेन तथा नाइट्रस ऑक्साइड गैसें दीर्घ तरंग दैर्ध्व वाली ताप विकिरणों को वायुमण्डल से बाहर नहीं जाने देतीं, इससे तापमान में होने वाली वृद्धि को हरित गृह प्रभाव कहते हैं।
प्रश्न 8.
अम्ल वर्षा के लिए उत्तरदायी कौनसी गैसें हैं?
उत्तर: सल्फर डाइऑक्साइड (SO2) तथा नाइट्रोजन डाइऑक्साइड (NO2).
प्रश्न 9.
ओजोन कवच को प्रभावित करने वाली प्रमुख गैस कौनसी है?
उत्तर: फ्रेऑन अर्थात् क्लोरोफ्लुओरो कार्बन।
प्रश्न 10.
स्मॉग किन अवयवों के मिलने से बनता है?
उत्तर: स्मॉग, स्मोक तथा फोग (धुआँ तथा कोहरे) के मिलने से बनता है।
प्रश्न 11.
पृथ्वी के वायुमण्डल में किस गैस की मात्रा सर्वाधिक है?
उत्तर: पृथ्वी के वायुमण्डल में नाइट्रोजन गैस की मात्रा सर्वाधिक है।
प्रश्न 12.
मुख्य औद्योगिक वायु प्रदुषक कौनसे हैं?
उत्तर: मुख्य औद्योगिक वायु प्रदूषक सल्फर, नाइट्रोजन कार्बन के ऑक्साइड तथा हाइड्रोकार्बन हैं। जो कि क्रमशः SO2, SO3, NO, NO2CO तथा CO2 हैं।
प्रश्न 13.
ग्रीन हाउस प्रभाव के लिए कौन सी गैस उत्तरदायी है?
उत्तर: कार्बन डाइऑक्साइड, मेथेन, नाइट्रस ऑक्साइड, जल वाष्प तथा क्लोरोफ्लुओरो कार्बन (फ्रेऑन) ग्रीन हाउस प्रभाव के लिए उत्तरदायी है।
प्रश्न 14.
जल प्रदूषण कितने प्रकार के होते हैं?
उत्तर: जल प्रदूषण तीन प्रकार के होते हैं –
- रोगजनक
- प्राकृतिक स्रोतों से
- मानव जनित स्रोतों से।
RBSE Class 11 Chemistry Chapter 14 लघूत्तरात्मक प्रश्न
प्रश्न 15.
वायु प्रदूषण के मुख्य स्रोत कौनसे हैं?
उत्तर: वायु प्रदूषण के मुख्य स्रोत दो प्रकार के होते हैं –
- कणीय
- गैसीय
1. कणीय – वाष्प कण कोहरा, ऐरोसोल, धुआं, धूल, कज्जल, धूम्र, धूमिका तथा सूक्ष्म बूंदें कणीय प्रदूषक हैं।
2. गैसीय –
- अकार्बनिक गैसें – क्लोरीन, कार्बन डाइऑक्साइड, ओजोन, हाइड्रोजन सल्फाइड, अमोनिया, नाइट्रिक ऑक्साइड, सल्फर के ऑक्साइड तथा कार्बन मोनोऑक्साइड आदि।
- कार्बनिक पदार्थ ऐल्डिहाइड ऐसीटिलीन, प्रोपेन, मेथेन, एथेन, हाइड्रोकार्बन, ऐल्कोहॉल इत्यादि।
प्रश्न 16.
स्मॉग किस प्रकार बनता है तथा इसके कुप्रभाव क्या हैं?
उत्तर:
धूम कोहरा ‘धूम’ तथा ‘कोहरा’ दो शब्दों से मिलकर बना है, अर्थात् यह इन दोनों का मिश्रण है। (स्मोग = स्मोक + फोग) सामान्य धूम कोहरा (अपचायक धूम कोहरा) ठण्डी तथा नम जलवायु में उत्पन्न होता है तथा यह धूम, कोहरे एवं सल्फर डाइऑक्साइड का मिश्रण होता है। प्रकाश रासायनिक धूम कोहरा (ऑक्सीकारक स्मॉग) ऊष्ण, शुष्क एवं साफ जलवायु में बनता है। यह स्वचालित वाहनों एवं कारखानों से निकलने वाले नाइट्रोजन के ऑक्साइडों तथा हाइड्रोकार्बनों पर सूर्य के प्रकाश की क्रिया के कारण उत्पन्न होता है।
प्रकाश रासायनिक धूम – कोहरे के कुप्रभाव –
- यह धातुओं, पत्थरों, भवन – निर्माण सामग्री तथा रंगी हुयी सतहों का संक्षारण करता है।
- ओजोन तथा नाइट्रिक ऑक्साइड नोक एवं गले में जलन पैदा करते हैं।
- इनकी उच्व सान्द्रता से सरदर्द, छाती में दर्द, गले का शुष्क होना, खाँसी एवं श्वास अवरोध हो सकता है।
- यह पौधों पर हानिकारक प्रभाव डालता है।
प्रश्न 17.
अम्ल वर्षा का क्या अर्थ है तथा यह पर्यावरण प्रदूषण को किस प्रकार प्रभावित करती है?
उत्तर:
अम्ल वर्षा – जब वर्षा जल की pH 5.6 से कम हो जाती है, तो इसे अम्ल वर्षा कहते हैं। अम्लीय वर्षा के निम्नलिखित दुष्प्रभाव होते हैं, अत: यह पर्यावरण प्रदूषण को प्रभावित करती है –
- जलीय प्राणियों की मृत्यु।
- पेड़ – पौधों की वृद्धि के गिरावट।
- तांबा, सीसा आदि घातक तत्त्वों का जल में मिल जाना।
- मिट्टी की अम्लीयता में वृद्धि तथा मिट्टी में उपस्थित पोषक तत्त्वों (Ca, K, Fe, Mn) का अम्ल वर्षा के साथ बहकर जाना जिससे, मृदा की उर्वरा शक्ति में गिरावट होना।
- संगमरमर तथा चूने के पत्थर की बनी इमारतों तथा स्मारकों जैसे आगरा में स्थित ऐतिहासिक इमारत ताजमहल आदि पर अम्ल वर्षा का अत्यधिक प्रभाव पड़ता है क्योंकि सल्फ्यूरिक अम्ल तथा नाइट्रिक अम्ल दोनों ही संगमरमर को घोलकर क्रमश: CaSO4 तथा Ca(NO3)2 बनाते हैं।
CaCO3 + H2SO4 → CaSO4 + CO2 + H2O
CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O
ये लवण जल के साथ धीरे – धीरे बह जाते हैं अतः इन स्मारकों का धीरे – धीरे क्षरण होता जा रहा है।
प्रश्न 18.
ग्रीन हाऊस प्रभाव क्या है तथा यह जीवन को किस प्रकार प्रभावित करता है?
उत्तर:
पृथ्वी के वातावरण में मौजूद कार्बन डाइऑक्साइड, मेथेन तथा नाइट्रस ऑक्साइड आदि गैसें दीर्घ तरंग दैर्ध्व वाली ताप विकिरणों को वायुमण्डल से बाहर नहीं जाने देतीं। इस कारण तापमान में होने वाली वृद्धि को हरित गृह प्रभाव कहते हैं। पृथ्वी से होने वाला ताप का परावर्तन दीर्घ तरंगों द्वारा होता है जो वायुमण्डल में उपस्थित बादलों, जल वाष्प, कार्बन डाइऑक्साइड गैस आदि द्वारा सोख लिया जाता है। अतः आकाश स्वच्छ रहने पर पृथ्वी से दीर्घ तरंगीय विकिरण सुगमता से हो जाता है और निचले वायुमण्डल में तापमान बढ़ने नहीं पाता है। किन्तु मेघाच्छादित आकाश रहने पर विकिरण की दीर्घ तरंगें उसे पार नहीं कर पाती हैं तथा जलवाष्प, धूलकण, कार्बन डाईऑक्साइड आदि उसे वापस नीचे की ओर लौटा देते हैं। पृथ्वी के समीप वायुमण्डल में तापमान उसी प्रकार सुरक्षित रहता है जिस प्रकार शीशा (कांच) से आवरित पौधघर में हरे पौधों के लिए तापमान आरक्षित रहता है।
ग्रीन हाउस प्रभाव का जीवन पर प्रभाव –
- प्रदूषण के बढ़ने से वायुमण्डल में हरित गृह प्रभाव को बढ़ाने वाली गैसों में वृद्धि हुई जिसके कारण पृथ्वी के तापमान में भी वृद्धि हुई।
- अध्ययनों से यह ज्ञात हुआ है कि पृथ्वी की सतह का औसत तापमान पिछले 100 वर्षों में 0.08°C बढ़ गया है। जिसके कारण महासागरों का तापीय विस्तार हो गया है। परिणामस्वरूप सागर जल के स्तर में 12 से 27 सेंटीमीटर की वृद्धि हो गयी है।
- हरित गृह प्रभाव से मौसम चक्र का संतुलन बिगड़ने की संभावना है।
- तापमान के बढ़ने से बर्फ पिघलती है जिससे मानव जीवन को खतरा हो सकता है।
- खाद्यान्नों के उत्पादन पर भी इसका प्रभाव पड़ता है।
- इससे बहुत से संक्रामक रोग जैसे डेंगू, मलेरिया इत्यादि में वृद्धि हो जाती है।
प्रश्न 19.
ओजोन परत के अपक्षय के क्या प्रभाव हैं?
उत्तर:
ओजोन परत के अपक्षय के कारण होने वाले प्रभाव निम्न प्रकार हैं –
ओजोन परत के क्षय के कारण अधिकाधिक पराबैंगनी विकिरण क्षोभमण्डल में आते हैं, जिनके कारण त्वचा को जीर्णन, मोतियाबिंद, सनबर्न, त्वचा – कैंसर जैसी बीमारियाँ होती हैं तथा इससे पादपप्लवकों की मृत्यु एवं मत्स्य उत्पादन में कमी होती है। पौधों के प्रोटीन पराबैंगनी विकिरणों से आसानी से प्रभावित हो जाते हैं, जिससे कोशिकाओं में हानिकारक उत्परिवर्तन होते हैं, जिसके कारण पत्तियों के रन्ध्रों से जल का वाष्पीकरण बढ़ जाता है, अतः मिट्टी की नमी कम हो जाती है। बढ़े हुए पराबैंगनी विकिरण रंगों एवं रेशों को भी हानि पहुँचाते हैं, जिससे रंग जल्दी हल्के हो जाते हैं। पराबैंगनी विकिरणों से शिशुओं में भी विकृति उत्पन्न हो जाती है तथा न्यूक्लिक अम्ल को भी क्षति पहुँचती है।
प्रश्न 20.
जल प्रदूषण का पादपों पर क्या प्रभाव पड़ता है?
उत्तर:
जल प्रदूषण का पादपों पर पड़ने वाला प्रभाव निम्न हैं –
- जल में ऑक्सीजन वातावरण से या जलीय पौधों द्वारा प्रकाश संश्लेषण द्वारा पहुँचती है। रात्रि में प्रकाश संश्लेषण रुक जाता है किन्तु पौधे श्वसन करते रहते हैं जिससे जल में ऑक्सीजन की कमी हो जाती है। जल में यदि अधिक कार्बनिक पदार्थ उपस्थित हो तो सारी उपलब्ध ऑक्सीजन उपयोग में आ जाएगी जिससे जलीय जीवों तथा पादपों की मृत्यु हो सकती है। वायु जीवाणु (ऑक्सीजन की आवश्यकता वाले) कार्बनिक अपशिष्टों का विघटन करके जल को ऑक्सीजन रहित बना देते हैं।
- मनुष्य प्रत्यक्ष या परोक्ष रूप से कीटों, कवकों, खरपतवारों, सूक्ष्म जीवों आदि को नष्ट करने के लिए पीड़कनाशी का उपयोग करता है। इनसे जीव – जन्तु एवं पेड़ – पौधों में कई प्रकार के हानिकारक परिवर्तन दिखाई देने लगे हैं। इनके उपयोग से सम्पूर्ण खाद्य श्रृंखला एवं खाद्य चक्र ही प्रदूषित हो रहा है।
प्रश्न 21.
औद्योगिक बहिःस्त्राव क्या होता है तथा यह पर्यावरण को किस प्रकार प्रदूषित करता है।
उत्तर:
औद्योगिक इकाइयों द्वारा उत्पन्न विभिन्न प्रकार के अपशिष्ट वायुमण्डल, जल और मृदा को प्रदूषित करते हैं। औद्योगिक अपशिष्ट की श्रेणी उद्योग के प्रकार पर निर्भर करती है। अधिकतर प्रदूषक उद्योगों से निकलने वाले उत्प्रवाहियों से प्राप्त होते हैं, जिनमें कार्बनिक पदार्थ, अकार्बनिक लवण, निलंबित ठोस, उर्वरक आदि उपस्थित होते हैं। ये सभी ऊष्मा, जीवाणु एवं रोगजनकों के रूप में बाहर निकलते हैं। राजस्थान में जहाँ थर्मल पावर प्लांट है जैसे रावतभाटा (कोटा) से निकलने वाले उत्प्रवाही ऊष्मा, भारी धातुएँ, घुलनशील ठोस एवं अकार्बनिक पदार्थ होते हैं। जयपुर, कोटपूतली एवं अन्य स्थानों पर पेपर तथा पल्प उद्योगों द्वारा जो औद्योगिक उत्प्रवाही निकलते हैं वे जल की pH को प्रभावित करते हैं एवं COD, BOD के संतुलन को अनियमित करते हैं। जहाँ रबर उद्योग है वे क्लोराइड निलंबित घुलनशील ठोस उत्प्रवाही के रूप में वातावरण में मिश्रित करते हैं। स्टील उद्योग जो कि भिवाड़ी व अन्य औद्योगिक क्षेत्रों में उपस्थित है उनसे – अम्ल फीनोल, सायनोजन, लाइमस्टोन, तेलीय पदार्थ, सायनाइड, सायनेट आदि प्रदूषक के रूप में निकलते हैं।
ऑयल रिफाइनरीज के द्वारा अम्ल, ऐल्कली, रेजिन्स और पेट्रो ऑयल प्रदूषक के रूप में निकाले जाते हैं। पेस्टीसाइडस जो कि सभी बड़े शहरों के आस – पास पाए जाते हैं उनमें ऐरोमैटिक पदार्थ, अम्ल एवं कार्बनिक द्रव्य होते हैं। राजस्थान के जयपुर, उदयपुर एवं अन्य शहरों में सांश्लेषिक औषधियाँ तथा पूर्ववर्ती अणु बनाए जाते हैं, जिससे कई तरह के प्रदूषक वायुमण्डल, जल तथा मृदा को प्रदूषित कर रहे हैं। राजस्थान के सभी शहरों के औद्योगिक क्षेत्रों में कार्बनिक रसायन उद्योग स्थापित हैं जिनसे कई विषाक्त पदार्थ जैसे – फीनोल, अम्ल एवं क्षार प्रदूषक के रूप में निकलते हैं। जयपुर, उदयपुर, कोटा एवं अन्य शहरों में उर्वरक उद्योगों के द्वारा निकलने वाले अपशिष्टों में अमोनिया, फ्लोराइड्स, कार्बनिक पदार्थ, पोटैशियम, नाइट्रोजन तथा फॉस्फोरस के यौगिक होते हैं। राजस्थान के बहुत से शहरों में स्थापित डेयरी उद्योग अपशिष्ट के रूप में ग्रीसेज, वसाएँ, लेक्टोज, गलनीय ठोस एवं प्रोटीन्स उत्पन्न करते हैं। उदयपुर, राजसमन्द एवं अन्य जिलों में मार्बल उद्योग के कारण उत्पन्न मार्बल स्लरी मृदा तथा पानी का प्रदूषण करती है। भीलवाड़ा एवं अन्य टेक्सटाइल नगरों में रंग, फीनोल, फाइबर आदि का प्रदूषण व्याप्त है।
RBSE Class 11 Chemistry Chapter 14 निबन्धात्मक प्रश्न
प्रश्न 22.
जल प्रदूषण के मुख्य स्रोत कौनसे हैं? जल प्रदूषण को नियंत्रित करने हेतु क्या उपाय किये जा सकते हैं?
उत्तर:
जल प्रदूषण परिभाषा:
प्राकृतिक जल में किसी अवांछित बाह्य पदार्थ (अपशिष्ट) की उपस्थिति जिससे जल की गुणवत्ता में कमी आती है, उसे जल प्रदूषण कहते हैं।
जल प्रदूषण के स्रोत दो प्रकार के होते हैं –
- बिन्दु स्रोत
- अबिन्दु स्रोत।
1. प्रदूषण के आसानी से ज्ञात स्रोतों या स्थानों को बिन्दु स्रोत कहते हैं। जैसे – नगरपालिका पाइप या औद्योगिक अपशिष्ट विसर्जन पाइप, जहाँ से प्रदूषक जलस्रोत में प्रवेश करते हैं।
2. जल प्रदूषण के अबिन्दु स्रोत वे हैं जहाँ पर प्रदूषण के स्रोत को आसानी से नहीं पहचाना जा सके, जैसे – कृषि अपशिष्ट (खेतों, जानवरों तथा कृषि भूमि से), अम्ल वर्षा, तीव्र जल निकासी (गलियों, उद्यानों तथा लॉन) इत्यादि। नीचे दी गयी सारणी में जल के मुख्य प्रदूषक तथा उनके स्रोत दिए गए हैं –
मुख्य जल प्रदूषक तथा उनके स्रोत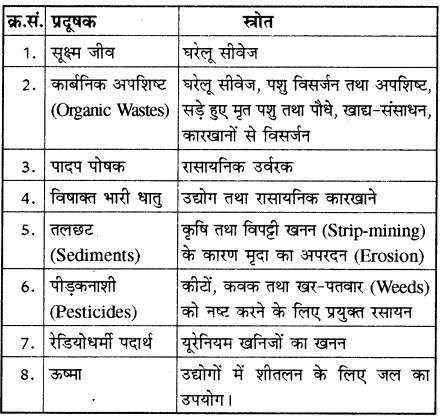
जल प्रदूषण के कारण:
जल का प्रदूषण मानवजनित तथा प्राकृतिक कारणों से होता है जो कि निम्न प्रकार हैं –
1. रोगजनक –
सबसे ज्यादा गम्भीर जल प्रदूषक रोग कारकों को रोगजनक कहते हैं। ये जीवाणु तथा अन्य जीव होते हैं। जो घरेलू सीवेज एवं पशु अपशिष्ट द्वारा जल में प्रवेश करते हैं। इश्चरेशिया कोलाई (एशारिकिआ कोलाई), स्ट्रेप्टोकॉकस फिकेलिस आदि जीवाणु मानव अपशिष्ट में होते हैं जिनसे जठरांत्र बीमारियाँ होती हैं।
2. प्राकृतिक स्रोतों से जल प्रदूषण –
जल प्रदूषण के प्राकृतिक स्रोतों के अन्तर्गत जन्तुओं का मल, पेड़ – पौधों और जन्तुओं के अवशेष, विभिन्न प्रकार के खनिज पदार्थों का खानों से निकलकर जल में मिश्रित होना, मृदाअपरदन इत्यादि आते हैं। बहते हुए जल में कई बार विषैली धातुएँ जैसे आर्सेनिक, सीसा, कैडमियम, पारा इत्यादि की मात्रा अधिक हो जाती है तो जल जहरीला हो जाता है।
3. मानवजनित स्रोतों से जल प्रदूषण –
(a) घरेलू अपशिष्ट पदार्थ –
(i) घरों से निकलने वाले अपशिष्ट में सड़े फल, सब्जियों के छिलके, पत्तियाँ, घास, कूड़ा – करकट, साबुन, अपमार्जक आदि होते हैं। सामान्यतया ये गंभीर प्रदूषण नहीं करते किन्तु आजकल इनमें कीटनाशक, फीनोल तथा अम्लीय पदार्थ उपस्थित होने से जल प्रदूषित और जहरीला हो रहा है।
(ii) जल में उपस्थित कणीय पदार्थ, अत्यन्त सूक्ष्म अघुलनशील पदार्थ, कोलॉइड, कार्बोहाइड्रेट, वसा, प्रोटीन, घुलनशील अपद्रव्य एवं सूक्ष्म जीव पाए जाते है। रसोईघरों, स्नानघरों तथा शौचालयों से निकलने वाली गंदगी भी प्रदूषक के रूप में रहती है।
(iii) जल की अधिक मात्रा का उपयोग, कारखानों में पानी की मांग, वस्त्र, कागज तथा रसायन उद्योगों में पानी की खपत दिन – प्रतिदिन बढ़ती जा रही है। प्रयोग के पश्चात् जल दूषित हो जाता है। इस तरह औद्योगीकरण की प्रगति के साथ – साथ जल प्रदूषण भी बढ़ता जा रहा है।
(iv) घरों तथा उद्योगों से निकले प्रदूषित जल को नदियों, नहरों तथा नालों में छोड़ दिया जाता है जिससे पानी के ये स्रोत प्रदूषित होते जा रहे हैं।
(v) नाइट्रोजन व फॉस्फोरस की मात्रा बढ़ने से तालाबों तथा समुद्रों में शैवालों की संख्या बढ़ रही है जिससे प्राकृतिक संतुलन बिगड़ने लगा है। जल में फ्लुओराइड की मात्रा अधिक होने से अस्थि रोग बढ़ने लगे हैं।
(b) वाहित मल द्वारा प्रदूषण – घरों, सार्वजनिक शौचालयों एवं नली नालों के किनारें, मानव एवं पशुओं के मल – मूत्र से प्रदूषित जल को वाहित मल या सीवेज कहते हैं। वाहित मल अधिकतर जैविक प्रदूषकों से युक्त होते हैं। इस संदूषण से विभिन्न बीमारियाँ जैसे हैजा, पेचिश, पीलिया, टाइफाइड, आंत्र शोध, अमीबायसिस आदि होने की संभावना रहती है।
(c) औद्योगिक बहिःस्राव द्वारा प्रदूषण – औद्योगिक इकाइयों से निकलने वाली घुलनशील गैसें तथा रसायन जल की बड़ी मात्रा को प्रदूषित करके अनुपयोगी बना रहे हैं।
(d) ताप द्वारा प्रदूषण – ताप बिजलीघर एवं अन्य रिएक्टरों के गर्म हो जाने पर तालाबों और बांधों के जल से ठण्डा करने की प्रक्रिया के कारण जल स्रोतों के ताप में वृद्धि हो जाती है। इससे जैविक संतुलन बिगड़ जाता है।
(e) कृषि अपशिष्ट द्वारा प्रदूषण – खेती में अधिक पैदावार प्राप्त करने के लिए रासायनिक उर्वरक, कीटनाशक जीवाणुनाशक आदि का उपयोग अधिक मात्रा में किया जा रहा है। इससे जल प्रदूषण बढ़ रहा है। कृषि क्षेत्र में उपर्युक्त रासायनिक पदार्थों में आर्सेनिक, सीसा, कैल्शियम, मर्करी गंधक, तांबा तथा फॉस्फोरस के यौगिक होते हैं।
(f) पीड़कनाशियों द्वारा प्रदूषण – मनुष्य प्रत्यक्ष या परोक्ष रूप से कीटों, कवकों, खरपतवारों, सूक्ष्म जीवों आदि को नष्ट करने के लिए पीड़कनाशी का उपयोग करता है। इनसे जीव – जन्तु एवं पेड़ – पौधों में कई प्रकार के हानिकारक परिवर्तन दिखाई देने लगे हैं। इनके उपयोग से सम्पूर्ण खाद्य श्रृंखला एवं खाद्य चक्र ही प्रदूषित हो रहा है।
(g) जैविक प्रदूषण – विभिन्न प्रकार के जीवाणु जल में उपस्थित रह कर दूसरे जीवों में बीमारियाँ उत्पन्न करके उन्हें नुकसान पहुंचाते हैं। बैक्टीरिया की बहुत अधिक संख्या जल में कार्बनिक पदार्थों का अपघटन करती है। ये जल में विलेय ऑक्सीजन का उपयोग करते हैं लेकिन जल में विलेय ऑक्सीजन की मात्रा सीमित होती है। ठण्डे जल में घुली हुई ऑक्सीजन की सान्द्रता 10 ppm तक होती है, जबकि वायु में यह लगभग 2 लाख ppm होती है। इसी कारण जल में थोड़े से कार्बनिक पदार्थ के अपघटित होने पर भी इसमें ऑक्सीजन की कमी हो जाती है। जल में घुली हुई ऑक्सीजन जलीय जीवन के लिए बहुत महत्त्वपूर्ण है। जब जल में घुली हुई ऑक्सीजन की सान्द्रता 6 ppm से कम हो जाती है, तो मछलियों का विकास रुक जाता है।
जल में ऑक्सीजन या तो वातावरण से या कई जलीय पौधों द्वारा होने वाले प्रकाश – संश्लेषण द्वारा पहुँचती है। रात में पौधों के श्वसन के कारण जल में घुली हुई ऑक्सीजन कम हो जाती है तथा सूक्ष्म जीवाणुओं द्वारा कार्बनिक यौगिकों के ऑक्सीकरण में भी ऑक्सीजन उपयोग में ली जाती है। यदि जल में बहुत अधिक कार्बनिक पदार्थ मिला दिए जाएँ, तो जल में उपलब्ध सारी ऑक्सीजन का उपभोग हो जाता है, जिससे ऑक्सीजन पर आश्रित जलीय जीवों की मृत्यु हो जाती है। इस प्रकार अवायु जीवाणु, जिन्हें ऑक्सीजन की आवश्यकता नहीं होती है, कार्बनिक अपशिष्ट का विखण्डन आरम्भ कर देते हैं तथा इससे दूषित गंध वाले रसायन उत्पन्न होते हैं, जो मनुष्य के स्वास्थ्य के लिए हानिकारक होते हैं। वायु जीवाणु (ऑक्सीजन की आवश्यकता वाले) इन कार्बनिक अपशिष्टों का विघटन करते हैं जिससे जल में घुली हुई ऑक्सीजन की मात्रा बहुत कम हो जाती है।
जैव रासायनिक ऑक्सीजन माँग तथा रासायनिक ऑक्सीजन माँग –
जल के एक नमूने के निश्चित आयतन में उपस्थित कार्बनिक पदार्थों को विखण्डित करने के लिए जीवाणु द्वारा आवश्यक ऑक्सीजन को जैव रासायनिक ऑक्सीजन माँग (BOD) कहा जाता है। अतः BOD, जल में उपस्थित कार्बनिक पदार्थ को जैवीय रूप में विखण्डित करने के लिए आवश्यक ऑक्सीजन की मात्रा होती है। BOD की गणना करने के लिए जल के नमूने को ऑक्सीजन से संतृप्त करके 293 K ताप पर 5 दिन तक रखते हैं जिससे जल में उपस्थित जीवाणु कार्बनिक पदार्थों (प्रदूषकों) को विखण्डित कर देते हैं। इस प्रक्रम में जल में उपस्थित ऑक्सीजन की कुछ मात्रा प्रयुक्त हो जाती है तथा शेष ऑक्सीजन का निर्धारण कर लिया जाता है। अतः BOD मान से जल की गुणवत्ता का निर्धारण होता है। मानक दशा में शुद्ध जल का BOD मान 5 ppm से कम होता है, जबकि अत्यधिक प्रदूषित जल में यह मान 17 ppm या इससे अधिक होता है। अतः। BOD का उच्च मान जल में कार्बनिक अपशिष्ट की उपस्थिति को दर्शाता है।
जल प्रदूषण को मापने का एक अन्य मापदण्ड रासायनिक ऑक्सीजन माँग COD है। कुछ रासायनिक पदार्थ भी जल में घुली हुई ऑक्सीजन से क्रिया करते हैं। COD की गणना करने के लिए जल को किसी ऑक्सीकारक (जैसे K2Cr2O7) की ज्ञात मात्रा के साथ अभिकृत करवाया जाता है तो यह कार्बनिक तथा अकार्बनिक प्रदूषकों को ऑक्सीकृत कर देता है। ऑक्सीकारक की शेष मात्रा का निर्धारण किसी उपयुक्त अपचायक द्वारा कर लिया जाता है जिससे प्रदूषकों के ऑक्सीकरण में प्रयुक्त ऑक्सीजन की मात्रा ज्ञात कर लेते हैं। यह मान ही COD कहलाता है तथा इसे भी ppm में व्यक्त किया जाता है।
(h) रासायनिक प्रदूषक –
जल एक अच्छा विलायक है अतः जल में विलेय अकार्बनिक रसायन तथा भारी धातुएँ जैसे मर्करी, कैडमियम तथा निकल (Cd, Hg, Ni) महत्त्वपूर्ण प्रदूषक हैं। ये सभी धातुएँ मनुष्य के लिए हानिकारक होती हैं, क्योंकि हमारा शरीर इनका विसर्जन नहीं कर पाता है। समय के साथ इनकी मात्रा निश्चित सीमा से ऊपर हो जाती है। तब ये प्रदूषक धातुएँ वृक्कों, केन्द्रीय तंत्रिका – तंत्र, यकृत आदि को नुकसान पहुँचाती हैं। खानों के सीवेज से प्राप्त अम्ल जैसे – सल्फ्यूरिक अम्ल एवं अनेक स्रोतों से प्राप्त लवण जिनमें ठण्डे मौसम में हिम एवं बर्फ को पिघलाने वाले लवण जैसे – सोडियम क्लोराइड एवं कैल्सियम क्लोराइड भी सम्मिलित हैं, जल में विलेय रासायनिक प्रदूषक हैं।
प्रदूषित जल में पाए जाने वाले कार्बनिक यौगिक प्रदूषकों का अन्य समूह है। पेट्रोलियम उत्पाद जैसे समुद्रों में बड़े तेल – बहाव जल के कई स्रोतों को प्रदूषित करते हैं, दूसरे गम्भीर प्रभाव वाले कार्बनिक यौगिक कीटनाशक हैं, जो स्प्रे द्वारा बहकर भूमि के नीचे आ जाते हैं। विभिन्न औद्योगिक रसायन, जैसे-पॉलीक्लोरीनेटेड बाइफिनायल (PCB8), अपमार्जक तथा उर्वरक भी जल – प्रदूषक होते हैं। PCB8 को कैन्सरजन्य माना जाता है। अधिकांश अपमार्जक जैव अपघटनीय होते हैं। फिर भी इनका प्रयोग कई समस्याएँ उत्पन्न करता है। अपमार्जकों को अपघटित करने वाले जीवाणु इन अपमार्जकों से भोजन प्राप्त करके तेजी से बढ़ते – हैं, जिससे वे जल में उपस्थित समस्त ऑक्सीजन का उपयोग करते हैं। जिसके कारण जल में ऑक्सीजन की कमी हो जाती है।
ऑक्सीजन की कमी के कारण जलीय जीवन (जैसे-मछलियाँ तथा पौधे) मर जाते हैं। उर्वरकों में फॉस्फेट योगज के रूप में होते हैं। जल में फॉस्फेट की वृद्धि शैवाल की वृद्धि में सहायक होती है। शैवाल की यह बढ़ोतरी जलीय सतह को ढक लेती है जिससे जल में ऑक्सीजन की सान्द्रता बहुत कम हो जाती है। अतः अवायुवीय परिस्थिति उत्पन्न होने से दुर्गंध युक्त सड़न पैदा होती है तथा यह जलीय जन्तुओं की मृत्यु का कारण बनती है। इस प्रकार यह पुष्पकुंजग्रस्त जल अन्य जीवों की वृद्धि को रोकता है। अतः वह प्रक्रम जिसमें पोषकों से युक्त जल निकाय, पादपों की सघन वृद्धि में सहयोग करता है जिससे ऑक्सीजन की कमी होकर जन्तुओं की मृत्यु हो जाती है तथा जैव विविधता में कमी आती है, उसे सुपोषण कहते हैं।
विभिन्न प्रदूषक धातुएँ तथा उनके प्रभाव निम्न प्रकार हैं –
- मर्करी – मर्करी सामान्य ताप पर द्रव अवस्था में पाया जाने वाला धातु है जो कि तापमान बढ़ने के साथ वाष्पित होता है तथा अधिक जहरीला होता जाता है। इसके द्वारा उत्पन्न मिनीमाटा नामक बीमारी से जापान में कई परिवारों एवं जानवरों की रहस्यमय मृत्यु हो गयी थी।
- सीसा – इसके प्रदूषण से यकृत तथा वृक्क की कार्यक्षमता प्रभावित होती है, हीमोग्लोबिन कम हो जाता है तथा मानसिक विक्षिप्तता आती है।
- आर्सेनिक – यह लीवर सिरोसिस नामक जानलेवा बीमारी उत्पन्न करता है, फेफड़ों का कैंसर, वृक्कों की कार्यक्षमता का ह्रास तथा मानसिक विक्षिप्तता पैदा करता है।
- कैडमियम – यह वृक्कों पर अवांछित प्रभाव, हड्डियों की विकृति, खून की कमी, केन्द्रीय तंत्रिका तंत्र एवं लीवर को नुकसान पहुँचाता है।
- तांबा – इससे तनाव व बुखार होता है तथा इसके अधिक मात्रा में पहुँचने पर व्यक्ति कोमा में भी चला जाता है।
- जिंक – यह वृक्कों को नुकसान पहुँचाता है तथा इससे उल्टी तथा ऐंठन आदि हो जाती है।
जल प्रदूषण का नियंत्रण:
निम्नलिखित प्रक्रियाओं द्वारा जल प्रदूषण को नियंत्रित किया जा सकता है –
- पेयजल को अपमार्जक, साबुन इत्यादि के प्रयोग से सुरक्षित रखा जाए अर्थात् कुआँ, तालाब इत्यादि पर इनका प्रयोग प्रतिबन्धित किया जाए।
- वाहित मल को जलस्रोतों में न मिलने दिया जाए।
- नाभिकीय अथवा प्रौद्योगिक संस्थानों से निकलने वाले अपशिष्ट पदार्थों को जलस्रोतों से दूर रखना चाहिए अथवा उन्हें बिना उपचार के जलस्रोतों में नहीं मिलाया जाना चाहिए।
- कृषि रसायन, कीटनाशक तथा उर्वरकों को जल में नहीं मिलाया जाना चाहिए।
- डी.डी.टी. तथा मैलाथियोन जैसे कीटनाशी के प्रयोग से बचना चाहिए तथा इनके स्थान पर नीम की सूखी पत्तियों का प्रयोग करना चाहिए।
- पेट्रोलियम तथा तेल पदार्थों को समुद्र में फैलने से बचाना चाहिए।
- रेडियोधर्मी पदार्थों को समुद्र में डालने तथा समुद्र में परमाणु विस्फोट पर प्रतिबंध लगाना चाहिए।
- नदी, तालाब तथा नहरों के पास मलमूत्र त्यागने पर पाबंदी लगानी चाहिए।
- रासायनिक उर्वरकों के स्थान पर कंपोस्ट का प्रयोग करना चाहिए।
- मृत जन्तु, मनुष्य तथा उनकी अस्थि इत्यादि को जल में प्रवाहित नहीं किया जाना चाहिए।
- जल को स्वच्छ करने वाली मछलियाँ, कछुए, घोंघा इत्यादि को जल में डालने पर ये जलस्रोतों के प्रदूषण को कम करते हैं।
- घरेलू पानी की टंकियों में पोटेशियम परमैंगनेट अथवा विरंजक चूर्ण (ब्लीचिंग पाउडर) की कुछ मात्रा समय – समय पर डालते रहना चाहिए।
- जनता को प्रदूषित जल से होने वाले खतरों के बारे में। टी.वी., रेडियो तथा मीडिया के अन्य स्रोतों द्वारा समय – समय पर जानकारी देते रहना चाहिए।
प्रश्न 23.
औद्योगिक वायु प्रदूषण पर एक लेख लिखें।
उत्तर:
औद्योगिक इकाइयों द्वारा उत्पन्न विभिन्न प्रकार के अपशिष्ट वायुमण्डल, जल और मृदा को प्रदूषित करते हैं। औद्योगिक अपशिष्ट की श्रेणी उद्योग के प्रकार पर निर्भर करती है। अधिकतर प्रदूषक उद्योगों से निकलने वाले उत्प्रवाहियों से प्राप्त होते हैं, जिनमें कार्बनिक पदार्थ, अकार्बनिक लवण, निलंबित ठोस, उर्वरक आदि उपस्थित होते हैं। ये सभी ऊष्मा, जीवाणु एवं रोगजनकों के रूप में बाहर निकलते हैं। राजस्थान में जहाँ थर्मल पावर प्लांट है जैसे रावतभाटा (कोटा) से निकलने वाले उत्प्रवाही ऊष्मा, भारी धातुएँ, घुलनशील ठोस एवं अकार्बनिक पदार्थ होते हैं। जयपुर, कोटपूतली एवं अन्य स्थानों पर पेपर तथा पल्प उद्योगों द्वारा जो औद्योगिक उत्प्रवाही निकलते हैं वे जल की pH को प्रभावित करते हैं एवं COD, BOD के संतुलन को अनियमित करते हैं। जहाँ रबर उद्योग है वे क्लोराइड निलंबित घुलनशील ठोस उत्प्रवाही के रूप में वातावरण में मिश्रित करते हैं। स्टील उद्योग जो कि भिवाड़ी व अन्य औद्योगिक क्षेत्रों में उपस्थित है उनसे – अम्ल फीनोल, सायनोजन, लाइमस्टोन, तेलीय पदार्थ, सायनाइड, सायनेट आदि प्रदूषक के रूप में निकलते हैं।
ऑयल रिफाइनरीज के द्वारा अम्ल, ऐल्कली, रेजिन्स और पेट्रो ऑयल प्रदूषक के रूप में निकाले जाते हैं। पेस्टीसाइडस जो कि सभी बड़े शहरों के आस – पास पाए जाते हैं उनमें ऐरोमैटिक पदार्थ, अम्ल एवं कार्बनिक द्रव्य होते हैं। राजस्थान के जयपुर, उदयपुर एवं अन्य शहरों में सांश्लेषिक औषधियाँ तथा पूर्ववर्ती अणु बनाए जाते हैं, जिससे कई तरह के प्रदूषक वायुमण्डल, जल तथा मृदा को प्रदूषित कर रहे हैं। राजस्थान के सभी शहरों के औद्योगिक क्षेत्रों में कार्बनिक रसायन उद्योग स्थापित हैं जिनसे कई विषाक्त पदार्थ जैसे – फीनोल, अम्ल एवं क्षार प्रदूषक के रूप में निकलते हैं। जयपुर, उदयपुर, कोटा एवं अन्य शहरों में उर्वरक उद्योगों के द्वारा निकलने वाले अपशिष्टों में अमोनिया, फ्लोराइड्स, कार्बनिक पदार्थ, पोटैशियम, नाइट्रोजन तथा फॉस्फोरस के यौगिक होते हैं। राजस्थान के बहुत से शहरों में स्थापित डेयरी उद्योग अपशिष्ट के रूप में ग्रीसेज, वसाएँ, लेक्टोज, गलनीय ठोस एवं प्रोटीन्स उत्पन्न करते हैं। उदयपुर, राजसमन्द एवं अन्य जिलों में मार्बल उद्योग के कारण उत्पन्न मार्बल स्लरी मृदा तथा पानी का प्रदूषण करती है। भीलवाड़ा एवं अन्य टेक्सटाइल नगरों में रंग, फीनोल, फाइबर आदि का प्रदूषण व्याप्त है।
प्रश्न 24.
ओजोन परत का क्या अर्थ है? इसके अपक्षय के कारण क्या हैं? ओजोन पर अपक्षय से पृथ्वी का जीवन किस प्रकार प्रभावित हो सकता है?
उत्तरे:
समतापमंडलीय प्रदूषण:
ओजोन का विरचन एवं विघटन –
ऊपरी समताप – मण्डल (समुद्र तल से 10 – 50 km ऊपर तक का क्षेत्रफल) में ओजोन प्रचुर मात्रा में होती है। इसके अतिरिक्त N2, O2 तथा सूक्ष्म मात्रा में जल वाष्प भी पायी जाती है। ओजोन सूर्य से आने वाली पराबैंगनी विकिरणों के 99.5 प्रतिशत भाग को रोककर हमें इन हानिकारक विकिरणों से बचाती है। इन विकिरणों से त्वचा – कैंसर (मेलेनोमा) होता है। अतः ओजोन – कवच को बचाए रखना आवश्यक है। समतापमण्डल में पराबैंगनी विकिरणों की ऑक्सीजन से क्रिया द्वारा ओजोन का निर्माण होता है। पराबैंगनी विकिरण आण्विक ऑक्सीजन को मुक्त ऑक्सीजन (O) परमाणुओं में विखण्डित कर देते हैं। जो कि आण्विक ऑक्सीजन से संयुक्त होकर ओजोन बनाते हैं।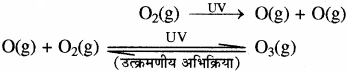
ओजोन ऊष्मागतिकीय रूप से अस्थायी होती है एवं यह आण्विक ऑक्सीजन में विघटित हो जाती है। इस प्रकार ओजोन के निर्माण एवं विघटन के मध्य एक गतिक साम्य स्थापित हो जाता है। अभी हाल ही के वर्षों में समतापमण्डल में उपस्थित कुछ रसायनों के कारण ओजोन की इस सुरक्षा-परत का क्षय होना प्रारम्भ हो गया है। ओजोन परत के इस क्षय का मुख्य कारण क्लोरोफ्लोरोकार्बन (फ्रेऑन) (CFCs) का उत्सर्जन है। फ्रेऑन अक्रिय, अज्वलनशील तथा अविषाक्त पदार्थ हैं, अतः इन्हें रेफ्रिजरेटर, एयर – कंडीशनर, प्लास्टिक फोम के निर्माण में एवं इलेक्ट्रॉनिक उद्योग में कम्प्यूटर के पुर्षों की सफाई करने में प्रयुक्त किया जाता है। सामान्यतः ताप तथा दाब की परिस्थितियों में भूमध्य रेखा के ऊपर ओजोन की सांद्रता 0.29 cm और ध्रुवों पर यह 0.40 cm तक पायी जाती है।
वायुमण्डल में एक बार फ्रेऑन के उत्सर्जित होने पर ये वायुमण्डल की अन्य गैसों के साथ मिलकर सीधे समतापमण्डल में पहुँच जाते हैं। समतापमण्डल में ये शक्तिशाली पराबैंगनी विकिरणों द्वारा विघटित होकर क्लोरीन मुक्त मूलक बनाते हैं।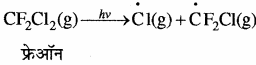
क्लोरीन मुक्त मूलक समतापमण्डल में स्थित ओजोन से अभिक्रिया करके क्लोरीन मोनोऑक्साइड मूलक ((dot { C } )lO) तथा आण्विक ऑक्सीजन बनाते हैं।![]()
क्लोरीन मोनोऑक्साइड मूलक परमाण्वीय ऑक्सीजन के साथ अभिक्रिया करके अधिक क्लोरीन मूलक उत्पन्न करता है।![]()
इस प्रकार क्लोरीन मूलक लगातार बनते रहते हैं तथा ओजोन को विखण्डित करते रहते हैं। अतः CFC समतापमण्डल में क्लोरीन मूलकों को उत्पन्न करने वाले एवं ओजोन परत को क्षति पहुँचाने वाले परिवहनीय कारक हैं। ओजोन परत के क्षय के कारणों को खोजने के लिए शेरवुड रोलेण्ड मारियो मेलिना एवं पॉल क्रट्जन को सन् 1945 में रसायन शास्त्र के क्षेत्र में नोबल पुरस्कार से सम्मानित किया गया।
ओजोन छिद्र –
सन् 1980 में वायुमण्डलीय वैज्ञानिकों ने अंटार्कटिका पर कार्य करते हुए दक्षिणी ध्रुव के ऊपर ओजोन परत के क्षय के बारे में बताया जिसे सामान्य रूप से ‘ओजोन छिद्र’ कहा जाता है। गरमी में नाइट्रोजन डाइऑक्साइड तथा मेथेन क्रमशः क्लोरीन मोनोऑक्साइड तथा क्लोरीन परमाणुओं से अभिक्रिया करके क्लोरीन सिंक बनाते हैं, जो ओजोन – क्षय को काफी हद तक रोकता है।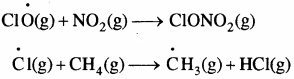
सर्दी के मौसम में अंटार्कटिका के ऊपर विशेष प्रकार के बादल बनते हैं जिन्हें ध्रुवीय समतापमण्डलीय बादल कहते हैं। ये बादल एक प्रकार की सतह प्रदान करते हैं जिस पर क्लोरीन नाइट्रेट जलअपघटित होकर हाइपोक्लोरस अम्ल बनाता है तथा उपरोक्त अभिक्रिया में उत्पन्न हाइड्रोजन क्लोराइड भी क्लोरीन नाइट्रेट से क्रिया करके आण्विक क्लोरीन देता है।
ClONO2(g) + H2O (g) → HOCl (g) + HNO3 (g)
ClONO2 (g) + HCl (g) → Cl2 (g) + HNO3 (g)
बसंत ऋतु में जब सूर्य का प्रकाश अंटार्कटिका पर आता है तो सूर्य की गर्मी से बादल विखण्डित हो जाते हैं तथा सूर्य के प्रकाश से HOCl तथा Cl2 का भी अपघटन हो जाता है।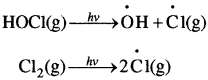
इस प्रकार उत्पन्न क्लोरीन मूलक, ओजोन क्षय के लिए श्रृंखला अभिक्रिया प्रारम्भ कर देते हैं।
उपरोक्त अभिक्रियाओं को सम्मिलित रूप से इस प्रकार लिखा जा सकता है –![]()
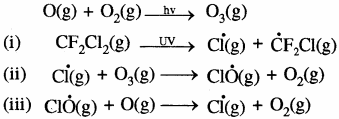
ओजोन परत के क्षय के प्रभाव:
ओजोन परत के क्षय के कारण अधिकाधिक पराबैंगनी विकिरण क्षोभमण्डल में छनित होते हैं, जिनसे त्वचा का जीर्णन, मोतियाबिंद, सनबर्न, त्वचा – कैंसर जैसी बीमारियाँ होती हैं तथा इससे पादपप्लवकों की मृत्यु तथा मत्स्य उत्पादन में कमी होती है। पौधों के प्रोटीन, पराबैंगनी विकिरणों से आसानी से प्रभावित हो जाते हैं, जिससे कोशिकाओं में हानिकारक उत्परिवर्तन होता है। इसके कारण पत्तियों के रंध्रों से जल का वाष्पीकरण बढ़ जाता है, जिससे मिट्टी की नमी कम हो जाती है। बढ़े हुए पराबैंगनी विकिरण रंगों एवं रेशों को भी हानि पहुंचाते हैं, जिससे रंग जल्दी हल्के हो जाते हैं। पराबैंगनी विकिरणों से शरीर के सम्पूर्ण प्रतिरोधी तंत्र की कार्यक्षमता में गिरावट आ जाती है। इनसे शिशुओं में भी विकृतियाँ उत्पन्न हो जाती हैं। ये विकिरण प्रकाश संश्लेषण की क्रिया को भी कम करते हैं। इनसे जैविक तत्त्वों के आनुवंशिक घटक न्यूक्लिक अम्ल को भी क्षति पहुँचती है तथा जीवन की खाद्य श्रृंखलाएँ अनियंत्रित हो जाती हैं। इस प्रकार इनसे सम्पूर्ण पारिस्थितिकी तंत्र पर विनाशकारी प्रभाव पड़ता है।
वायु प्रदूषण का नियन्त्रण –
निम्नलिखित उपायों द्वारा वायु प्रदूषण को काफी हद तक कम किया जा सकता है –
- वायु प्रदूषण का सार्थक नियन्त्रण ‘हरित क्रान्ति’ द्वारा सम्भव है।
- औद्योगिक चिमनियों से निकलने वाली गैसों को कार्बन से मुक्त करके वायुमण्डल में छोड़ा जाना चाहिए।
- सीमित क्षेत्र में ही विशेष प्रकार के प्रदूषण रहित उद्योगों को स्थापित किया जाना चाहिए।
- मोटर वाहनों में सीसारहित पेट्रोल का प्रयोग किया जाना चाहिए।
- वाहनों में उत्प्रेरकीय कन्वर्टर’ लगाकर प्रदूषण को कम करना चाहिए।
- C.N.G. गैसयुक्त वाहनों को ही चलने की अनुमति प्रदान की जानी चाहिए।
- ईंधन के रूप में गोबर गैस, बायो गैस इत्यादि का प्रयोग किया जाना चाहिए।
- यथासंभव जीवाश्म ईंधन के स्थान पर सौर ऊर्जा द्वारा चलित वाहनों का प्रयोग किया जाना चाहिए।
- कूड़ा और जैव – क्षय के पदार्थों को खुली वायु में नहीं छोड़ा जाना चाहिए।
- मानवीय – जागरूकता द्वारा भी वायु – प्रदूषण को कम किया जा सकता है। जैसे – लाल बत्ती संकेतक पर खड़े हजारों वाहन यदि इंजन को कुछ समय के लिए बन्द कर दें तो काफी मात्रा में वायु प्रदूषण कम हो सकता है।
प्रश्न 25.
वायु प्रदूषण के कारणों और निवारण पर लेख लिखें।
उत्तर:
वायुमण्डलं:
विश्व स्वास्थ्य संगठन (WHO) के अनुसार वायु प्रदूषण उन परिस्थितियों तक सीमित रहता है जहाँ बाहरी वायुमण्डल में दूषित पदार्थों की सान्द्रता मनुष्य एवं पर्यावरण को हानि पहुँचाने की सीमा तक बढ़ जाती है। वायुमण्डल के प्राकृतिक संघटन में किसी प्रकार का परिवर्तन वायुमण्डलीय प्रदूषण कहलाता है। वायुमण्डलीय प्रदूषण में मुख्यतः क्षोभमण्डलीय तथा समतापमण्डलीय प्रदूषण का अध्ययन किया जाता है। वायुमण्डल, जो कि पृथ्वी को चारों तरफ से घेरे हुए है, की मोटाई हर ऊँचाई पर समान नहीं होती है। इसमें वायु की विभिन्न संकेन्द्री परतें अथवा क्षेत्र होते हैं तथा प्रत्येक परत का घनत्व भिन्न – भिन्न होता है।
वायुमण्डल का सबसे निचला क्षेत्र, जिसमें मनुष्य तथा अन्य प्राणी रहते हैं, को क्षोभमण्डल’ कहा जाता है। यह समुद्र – तल से लगभग 10 किमी. की ऊँचाई तक होता है, इसके ऊपर (समुद्र – तल से 10 से 50 किमी. के मध्य) समतापमण्डल होता है। क्षोभमण्डल धूल के कणों से युक्त क्षेत्र होता है, जिसमें वायु, जलवाष्प (आधिक्य में) तथा बादल होते हैं। इस क्षेत्र में वायु का तीव्र प्रवाह होता है तथा बादलों का निर्माण होता है, जबकि समतापमण्डल में डाइनाइट्रोजन, डाइऑक्सीजन, ओजोन तथा सूक्ष्म मात्रा में जलवाष्प उपस्थित होती है।
समतापमण्डल में उपस्थित ओजोन सूर्य की हानिकारक पराबैंगनी किरणों के 99.5% भाग को पृथ्वी की सतह तक पहुँचने से रोकती है। तथा इसके प्रभाव से मानव तथा अन्य जीवों की रक्षा करती है। सामान्यतया वायु प्रदूषकों का उत्पत्ति के आधार पर अध्ययन किया जाता है –
(1) प्राथमिक – वे प्रदूषक जो वातावरण में ज्ञात प्रत्यक्ष स्रोतों से निष्कासित होते हैं तथा उसी अवस्था में अधिक समय तक स्थिर रहते हैं, उन्हें प्राथमिक प्रदूषक कहते हैं। जैसे – कार्बन मोनो ऑक्साइड, सल्फर डाइ ऑक्साइड, हाइड्रोकार्बन आदि।
(2) द्वितीयक – वे प्रदूषक जो प्राथमिक प्रदूषकों की आन्तरिक क्रियमों अथवा वायुमण्डल के साथ प्रक्रियाओं द्वारा निर्मित होते हैं, उन्हें द्वितीयक प्रदूषक कहते हैं।
क्षोभमण्इलीय प्रदूषण:
वायु में उपस्थित अवांछनीय ठोस अथवा गैस कणों के कारण क्षोभमण्डलीय प्रदूषण होता है। क्षोभमण्डल में मुख्यतः निम्नलिखित गैसीय तथा कणिकीय प्रदूषक पाए जाते हैं –
(1) कणीय आधार – वाष्प कण, कोहरा, ऐरोसोल, धुआं, धूल, कज्जल, धूम्र, धूमिका तथा सूक्ष्म बूंदें कणीय प्रदूषक हैं।
(2) गैसीय आधार
(i) अकार्बनिक गैसें – क्लोरीन, कार्बन – डाइऑक्साइड, ओजोन, हाइड्रोजन सल्फाइड, अमोनिया, नाइट्रिक ऑक्साइड, सल्फर के ऑक्साइड तथा कार्बन मोनो ऑक्साइड।
(ii) कार्बनिक पदार्थ ऐल्डिहाइड ऐसीटिलीन, प्रोपेन, मेथेन, एथेन, हाइड्रोकार्बन, ऐल्कोहॉल इत्यादि।
गैसीय वायु प्रदूषक –
(1) सल्फर के ऑक्साइड – जीवाश्म ईंधन के दहन से सल्फर के ऑक्साइड (SO2 तथा SO3) उत्पन्न होते हैं, इनमें सल्फर डाइऑक्साइड प्रमुख है जो कि मनुष्यों एवं जन्तुओं के लिए विषैली होती है। सल्फर डाइऑक्साइड की सूक्ष्म मात्रा भी मनुष्य में विभिन्न श्वसन रोग, जैसेअस्थमा, श्वसनी शोध, ऐम्फाइसीमा आदि उत्पन्न करती हैं। सल्फर डाइऑक्साइड के कारण आँखों में जलन भी होती है, जिससे आँखें लाल हो जाती हैं तथा आँसू आने लगते हैं। SO2 की उच्च सान्द्रता फूलों की कलियों में कड़ापन उत्पन्न करती है, जिससे ये शीघ्र पयावरणाय रसायन गिर जाती हैं। SO2 का ऑक्सीकरण धीमा होता है लेकिन प्रदूषित वायु जिसमें कणिकीय पदार्थ होते हैं, के कारण इसका ऑक्सीकरण तेजी से होता है अर्थात् ये इस अभिक्रिया को उत्प्रेरित करते हैं।
2SO2 (g) + O2 (g) → 2SO2 (g)
इस अभिक्रिया की गति वायुमण्डल में उपस्थित ओजोन तथा हाइड्रोजन परॉक्साइड द्वारा और बढ़ जाती है।
SO2 (g) + O2 (g) → SO3(g) + O2 (g)
SO2 (g) + H2O (g) → H2SO4 (aq)
इस प्रकार बनी SO3 तथा H2SO4 ही अम्ल वर्षा के लिए मुख्य रूप से उत्तरदायी है।
(2) नाइट्रोजन के ऑक्साइड –
वायु के प्रमुख अवयव नाइट्रोजन तथा ऑक्सीजन हैं। सामान्य ताप पर ये गैसें आपस में अभिक्रिया नहीं करती हैं, परन्तु जब आसमान में बिजली चमकती है, तब ये आपस में क्रिया करके नाइट्रोजन के ऑक्साइड (NO तथा NO2) बनाती हैं। NO2 के ऑक्सीकरण से NO3– आयन बनता है, जो मृदा में जाकर उर्वरक का कार्य करता है। किसी स्वचालित इंजन में भी उच्च ताप पर जब जीवाश्म ईंधन का दहन होता है, तो नाइट्रोजन तथा ऑक्सीजन मिलकर पर्याप्त मात्रा में नाइट्रिक ऑक्साइड (NO) तथा नाइट्रोजन डाइऑक्साइड (NO2) बनाती हैं।![]()
NO, ऑक्सीजन से तेजी से क्रिया करके NO2 देती है।
2NO (g) + O2 (g) → 2NO2 (g)
जब समतापमण्डल में नाइट्रिक ऑक्साइड (NO) ओजोन से क्रिया करती है, तो नाइट्रोजन डाइऑक्साइड (NO2) के बनने की दर बढ़ जाती है।
NO (g) + O3 (g) → NO2 (g) + O2 (g)
यातायात तथा सघन स्थानों पर स्थित तीक्ष्ण लाल धूम्र नाइट्रोजन ऑक्साइड के कारण ही होता है। NO2 की सान्द्रता अधिक होने पर पौधों की पत्तियाँ गिर जाती हैं तथा प्रकाश – संश्लेषण की दर कम हो जाती है। नाइट्रोजन डाइऑक्साइड फेफड़ों में उत्तेजना उत्पन्न करती है, जिससे बच्चों में श्वसन – रोग हो जाते हैं। यह जीव ऊतकों के लिए विषैली होती है। नाइट्रोजन डाइऑक्साइड विभिन्न प्रकार के रेशों तथा धातुओं के लिए भी हानिकारक होती है।
(3) हाइड्रोकार्बन –
हाइड्रोकार्बन केवल कार्बन तथा हाइड्रोजन से बने यौगिक हैं जो कि स्वचालित वाहनों में ईंधन के अपूर्ण दहन से उत्पन्न होते हैं। अधिकांश हाइड्रोकार्बनों के कारण कैंसर रोग उत्पन्न होता है। पौधों में काल प्रभावण, ऊतकों के निम्नीकरण पत्तियों एवं फूलों का असामयिक गिर जाना एवं पौधों तथा ऊतकों की वृद्धि में कमी आदि समस्याएँ इनके कारण ही उत्पन्न होती हैं।
कार्बन के ऑक्साइड –
कार्बन के तीन ऑक्साइड होते हैं। कार्बन मोनोऑक्साइड (CO), कार्बन डाइऑक्साइड (CO2), कार्बन सबऑक्साइड (C3O2)। इनमें से दो प्रकृति में पाए जाते हैं, कार्बन मोनोऑक्साइड और कार्बन डाइऑक्साइड।
(1) कार्बन मोनोऑक्साइड – कार्बन मोनोऑक्साइड एक गम्भीर वायु प्रदूषक है जो कि रंगहीन तथा गंधहीन गैस होती है। यह श्वसनीय प्राणियों के लिए हानिकारक है। यह कार्बन के अपूर्ण दहन के कारण उत्पन्न होती है। इसकी सर्वाधिक मात्रा मोटरवाहनों से निकलने वाले धुएँ में होती है। कोयला, ईंधन लकड़ी तथा पेट्रोल का अपूर्ण दहन इत्यादि इसके अन्य स्रोत हैं। अधिकतर वाहनों का उचित रखरखाव नहीं होता है। तथा इनमें प्रदूषण नियंत्रक उपकरण नहीं होते हैं जिसके कारण अत्यधिक मात्रा में कार्बन मोनोऑक्साइड तथा अन्य प्रदूषक गैसें उत्सर्जित होती हैं। कार्बन मोनोऑक्साइड अंगों तथा ऊतकों में जाने वाली ऑक्सीजन के प्रवाह को रोकती है।
यह हीमोग्लोबिन के साथ ऑक्सीजन की अपेक्षा अधिक प्रबलता से संयुक्त होकर कार्बोक्सीहीमोग्लोबिन बनाती है, जो कि ऑक्सीजन हीमोग्लोबिन (ऑक्सीहीमोग्लोबिन) संकुल से 320 गुना अधिक स्थायी होता है। जब रक्त में कार्बोक्सीहीमोग्लोबिन की मात्रा 3.6 प्रतिशत से अधिक हो जाती है, तो रक्त में ऑक्सीजन ले जाने की क्षमता कम हो जाती है। ऑक्सीजन की इस कमी से सिरदर्द, नेत्रदृष्टि में कमी, तंत्रिकीय आवेग में न्यूनता, हृदयवाहिका में अव्यवस्था आदि समस्याएँ उत्पन्न हो जाती हैं। इसी कारण धूम्रपान स्वास्थ्य के लिए हानिकारक है। गर्भवती महिलाओं के रक्त में CO की मात्रा बढ़ने से समय पूर्व बच्चे का जन्म, गर्भपात तथा बच्चों में विकृति उत्पन्न हो जाती है। CO की 1300 pprn सान्द्रता आधे घण्टे में प्राणघातक हो सकती है।
(2) कार्बन डाइऑक्साइड – श्वसन, जीवाश्म ईंधन, कार्बनिक पदार्थ का दहन, सीमेन्ट निर्माण में काम आने वाले चूना – पत्थर (CaCO3) आदि से कार्बन डाइऑक्साइड (CO2) उत्सर्जित होती है। कार्बन डाइऑक्साइड गैस केवल क्षोभमण्डल में होती है। सामान्यतः वायुमण्डल में इसकी मात्रा आयतन के अनुसार 0.03% होती है। कार्बन डाइऑक्साइड के आधिक्य को हरे पौधे प्रकाश संश्लेषण द्वारा कम कर देते हैं, जिससे वायुमण्डल में CO2 की निश्चित मात्रा बनी रहती है। हरे पौधे प्रकाश – संश्लेषण के लिए CO2 काम में लेते हैं तथा ऑक्सीजन मुक्त करते हैं इसलिए संतुलित चक्र बना रहता है। वनों के कटने तथा जीवाश्म ईंधन के अधिक दहन के कारण वायुमण्डल में CO2 की मात्रा बढ़ गई है अतः पर्यावरण – संतुलन बिगड़ गया है। हालांकि CO2 का कोई प्रत्यक्ष नकारात्मक प्रभाव नहीं होता लेकिन इसकी बढ़ी हुई मात्रा ही भूमण्डलीय तापवृद्धि तथा वैश्विक तापन के लिए उत्तरदायी है तथा आँकड़ों के अनुसार प्रतिदशक में CO2 की सान्द्रता निरंतर बढ़ती जा रही है।
भूमण्डलीय ताप वृद्धि तथा हरित गृह (ग्रीन हाउस) प्रभाव –
सौर ऊर्जा का 75% भाग पृथ्वी की सतह द्वारा अवशोषित कर लिया जाता है, जिससे इसके ताप में वृद्धि होती है। ऊष्मा – की शेष मात्रा वायुमण्डल में पुनः विकिरिंत हो जाती है। ऊष्मा का कुछ भाग वायुमण्डल में उपस्थित गैसों जैसे – कार्बन डाइऑक्साइड, ओजोन, क्लोरोफ्लोरोकार्बन (फ्रीऑन्स) तथा जलवाष्प द्वारा ग्रहण कर लिया जाता है, जिससे वायुमण्डल के ताप में वृद्धि होती है, इसे ही भूमण्डलीय ताप वृद्धि कहते हैं। ठण्डे स्थानों पर फल – फूल, सब्जियाँ आदि काँच के आवरण जिसे ‘हरितगृह’ कहते हैं, में विकसित किए जाते हैं। इसी प्रकार मनुष्य भी एक प्राकृतिक हरित गृह में रहता है, जो कि वायु का एक आवरण है, जिसे ‘वायुमण्डल’ कहते हैं, जिसके कारण शताब्दियों से पृथ्वी का ताप स्थिर है, परन्तु आजकल इसमें धीरे – धीरे परिवर्तन हो रहा है। जिस प्रकार हरितगृह में काँच सूर्य की गरमी को अन्दर थामे रखता है, उसी प्रकार वायुमण्डल भी सूर्य की ऊष्मा को पृथ्वी के निकट अवशोषित कर लेता है।
इससे पृथ्वी गरम रहती है अर्थात् इसके तापमान में वृद्धि होती है। इसे ‘प्राकृतिक हरितगृह प्रभाव’ कहते हैं, क्योंकि यह पृथ्वी के तापमान को संरक्षित करके उसे जीवन – योग्य बनाता है। दृश्यप्रकाश हरितगृह के पारदर्शी काँच में से गुजरकर, सूर्य के विकिरण द्वारा मृदा तथा पौधों को गरम रखता है। गरम मृदा तथा पौधे ऊष्मीय क्षेत्र के अवरक्त विकिरणों का उत्सर्जन करते हैं। चूँकि यह काँच विकिरण के लिए अपारदर्शक होता है, अतः यह इन विकिरणों को आंशिक रूप से अवशोषित तथा शेष को परावर्तित कर देता है। इस क्रियाविधि से हरितगृह में सौर – ऊर्जा संगृहीत रहती है। इसी प्रकार कार्बन डाइऑक्साइड के अणु ऊष्मा को संगृहीत कर लेते हैं, क्योंकि ये सूर्य के प्रकाश के लिए पारदर्शक होते हैं, ऊष्मा के विकिरणों के लिए नहीं। अतः जब कार्बन डाइऑक्साइड की मात्रा 0.03% से अधिक हो जाती है, तो प्राकृतिक हरितगृह का संतुलन बिगड़ जाता है। इसलिए भूमण्डलीय तापवृद्धि में कार्बन डाइऑक्साइड का विशिष्ट योगदान होता है।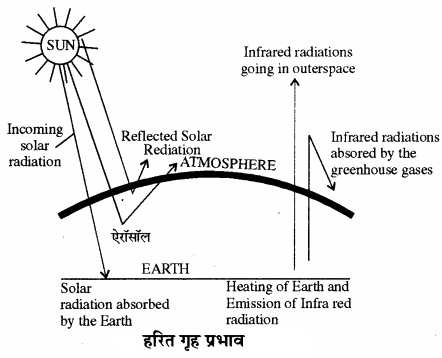
कार्बन डाइऑक्साइड के अतिरिक्त अन्य हरितगृह गैसें, मेथेन (CH4), जलवाष्प, नाइट्रसऑक्साइड (N2O), क्लोरोफ्लोरोकार्बन तथा ओजोन हैं। ऑक्सीजन की अनुपस्थिति में जब वनस्पतियों को जलाया या सड़ाया जाता है, तब मेथेन गैस उत्पन्न होती है। धान के क्षेत्रों, कोयले की खानों, दलदली क्षेत्रों तथा जीवाश्म ईंधनों द्वारा भी अधिक मात्रा में मेथेन उत्पन्न होती है। क्लोरोफ्लोरोकार्बन कृत्रिम रसायन है, जो वायुप्रशीतक आदि में काम आते हैं। ये भी ओजोन – परत को हानि पहुँचा रहे हैं। नाइट्रस ऑक्साइड (N2O) वातावरण में प्राकृतिक रूप से उत्पन्न होता है, परन्तु पिछले कुछ वर्षों में जीवाश्म ईंधन एवं उर्वरकों के अधिक प्रयोग से इसकी मात्रा में काफी वृद्धि हुई है।
वायुमण्डल जनित सूर्यातप प्रभाव पृथ्वी के तापमान को नियंत्रित करने में सहायक होता है। सौर विकिरण की लघु तरंगें वायुमण्डल को सुगमतापूर्वक पार करके पृथ्वी तक पहुँच जाती हैं। पृथ्वी से होने वाले ताप का परावर्तन दीर्घ तरंगों द्वारा होता है जो कि वायुमण्डल में उपस्थित बादलों, जल वाष्प तथा कार्बन डाइऑक्साइड गैसों द्वारा सोख लिया जाता है। इसी कारण आकाश स्वच्छ रहने पर पृथ्वी से दीर्घ तरंगीय विकिरण सुगमता से हो जाता है और निचले वायुमण्डल का तापमान नहीं बढ़ पाता है। किन्तु मेघाच्छादित आकाश रहने पर विकिरण की दीर्घ तरंगें उसे पार नहीं कर पाती हैं तथा जलवाष्प, धूलकण, कार्बन डाइऑक्साइड आदि उसे वापस नीचे की ओर लौटा देते हैं।
पृथ्वी के समीप वायुमण्डल का तापमान उसी प्रकार सुरक्षित रहता है, जिस प्रकार काँच से आवरित पौध गृह में हरे पौधों के लिए तापमान आरक्षित रहता है। पौध गृह प्रभाव के कारण ही आकाश स्वच्छ रहने पर रातें अपेक्षाकृत ठंडी होती हैं और आकाश मेघाच्छादित रहने पर गर्म रहती हैं। धरती के वातावरण के तापमान को प्रभावित करने वाले अनेक कारक हैं जिनमें से ग्रीन हाउस प्रभाव भी एक है। ग्रीन हाउस प्रभाव की खोज सन् 1824 में जोसेफ फुरिअर ने की थी। इस पर विश्वसनीय ढंग से प्रयोग सन् 1858 में जॉन टिण्डल ने किया। किन्तु सबसे पहले इसके बारे में आंकिक जानकारी सन् 1896 में स्वान्ते अर्हिनिअस ने प्रकाशित की।
हमारी पृथ्वी की जलवायु सूर्य की ऊष्मा द्वारा जीवन पाती है। अर्थात् सूर्य से उत्पन्न ऊर्जा का मानव जीवन से सीधा सम्बन्ध होता है। यह प्रकृति के प्रारम्भ से लेकर वर्तमान तक (लगभग चार अरब वर्षों) वृहद् श्रृंखला प्रक्रिया के तहत चलता रहता है। सूर्य से ली गयी विकिरण ऊर्जा पृथ्वी पर उत्सर्जित भी होती रहती है। इस प्रक्रिया से पृथ्वी अतिरिक्त ऊर्जा से सुरक्षित भी रहती है। बार – बार विकीर्णन एवं उत्सर्जन की प्रक्रिया में पर्यावरण से कुछ रेडियोएक्टिव किरणें, इनसे ऊर्जा शोषित कर लेती है और कुछ गैसे निकाल देती है। इस प्रक्रिया से निकलने वाली कुछ हरित गृह गैसें होती हैं, जिनका निर्माण जलवाष्प पानी के वाष्पन से होता है। अतः स्पष्ट है कि “हरित गृह प्रभाव वह क्रिया है। जो पार्थिव विकिरण को वायुमण्डल द्वारा रोक लिए जाने के कारण पृथ्वी के तापमान बढ़ने से सम्बन्धित है।”
हरित गृह प्रभाव के परिणाम – हरित गृह प्रभाव के परिणाम निम्नलिखित हैं –
- प्रदूषण के बढ़ने से वायुमण्डल में हरित गृह प्रभाव को बढ़ाने वाली गैसों में वृद्धि हुई जिसके कारण पृथ्वी में तापमान में भी वृद्धि हुई।
- अध्ययनों से यह ज्ञात हुआ है कि पृथ्वी की सतह का औसत तापमान पिछले 100 वर्षों में 0.08°C बढ़ गया है, जिसके कारण महासागरों का तापीय विस्तार हो गया है। परिणामस्वरूप सागर जल के स्तर में 12 से 27 सेंटीमीटर की वृद्धि हो गयी है।
- अगर इसी प्रकार से महासागरों का तापीय विस्तार होता गया तो जल चक्र पर कुप्रभाव पड़ने की आशंका है और जल चक्र के असंतुलित होने पर पूरे पारितंत्र के चक्र पर भी कुप्रभाव पड़ेगा।
- मानव की प्रकृति विरोधी नीतियों एवं कार्यों के कारण संतुलित वातावरण (जलवायु) में परिवर्तन हो रहा है और इसी संदर्भ में हरित गृह प्रभाव उत्पन्न करने वाली प्रमुख गैसों की मात्रा वायुमण्डल में आवश्यकता से अधिक बढ़ गयी है। जिससे पृथ्वी का तापमान औसत से अधिक बढ़ता जा रहा है और यदि यही स्थिति जारी रही तो आने वाले समय में पृथ्वी के प्राणी जगत, वनस्पति जगत एवं मौसम चक्र का संतुलन बिगड़ जायेगा।
- हरित गृह प्रभाव के बारे में यूरोप के भू – वैज्ञानिकों ने एक संगोष्ठी के माध्यम से (1986) में भविष्यवाणी की कि सन् 2050 तक पृथ्वी के तापमान में 1.5 से 4.5 डिग्री सेन्टीग्रेड की वृद्धि होने की सम्भावना है, और वर्तमान में इसके दुष्परिणाम भी सामने आने लगे हैं।
- मार्च 2002 में लंदन के वैज्ञानिकों ने सुदूर संवेदन उपग्रह से प्राप्त आंकड़ों के आधार पर बताया कि अण्टार्कटिका के पूर्वी प्रायद्वीप भाग से जुड़ा लार्सन बी हिमनद टूट गया है। 1250 वर्ग मील क्षेत्रफल एवं 650 फुट मोटाई वाली बर्फ की इस चट्टान के टूटने को, दुनिया के लिए खतरा बताया जा रहा है।
- पृथ्वी के बढ़ते तापमान से जहाँ एक ओर बर्फ के पिघलने की इन घटनाओं ने मानव को खतरे में डाल दिया है वहीं पिघली बर्फ का पानी जब सागरों में आएगा तो उसमें बाढ़ आ जाने से भारत एवं विश्व के कोलकाता, मुम्बई, बैंकॉक, बोस्टन, ढाका जैसे शहर जो समुद्र तट पर बसे हैं समुद्र की चपेट में आकर डूब जायेंगे।
- खाद्यानों के उत्पादन में हरित गृह प्रभाव का भी असर होता है। एक निश्चित तापमान न मिलने के कारण उत्पादन कम होता है। क्योंकि 15 से 4.5 डिग्री सेल्सियस ताप में वृद्धि होने से ताप, दाब एवं आर्द्रता की स्थितियों में परिवर्तन के कारण क्षेत्रीय जलवायु में परिवर्तन होता है जिससे फसलों के उत्पादन तथा फसल चक्र में परिवर्तन होंगे जिससे अमेरिका, भारत, आस्ट्रेलिया पूर्वोत्तर अफ्रीका व मध्य – पूर्व के देशों की अर्थव्यवस्थाएँ प्रभावित होंगी।
- इसके साथ ही मौसम के इस परिवर्तन से क्षेत्रीय पारिस्थितिक तंत्र भी लड़खड़ा जायेगा और वहाँ की घास, वनस्पतियाँ तो नष्ट होंगी ही साथ में पशु-पक्षियों का क्षेत्र भी बदल जायेगा।
- वैश्विक परिवेश में अलनीनो की ठण्डी जल धारा जो अमेरिका (दक्षिणी) के तट पर बहती थी अब वह गर्म हो गयी है जिससे इसमें रहने वाले जीवों को अनेक कष्ट उठाने पड़ रहे हैं।
- भूमण्डलीय तापवृद्धि के कारण बहुत से संक्रामक रोगों, जैसे – डेंगू, मलेरिया, पीत ज्वर, निद्रा रोग आदि में भी वृद्धि हो जाती है।
हरित गृह प्रभाव के संरक्षण के उपाय – (भूमण्डलीय ताप वृद्धि को कम करने के उपाय) –
हरित गृह प्रभाव का संरक्षण करने के लिए वर्तमान में बढ़ती हुई उपभोक्तावादी संस्कृति का प्रसार विश्व स्तर पर रोका जाना चाहिए। प्रकृति से स्नेह रखते हुए मानव को सादगीपूर्ण जीवन जीना चाहिए। यह एक ऐसी जागरूकता है जो किसी के दबाव में नहीं हो सकती है बस इसके लिए जरूरत है केवल दृढ़ इच्छा शक्ति की। इसके अतिरिक्त कुछ सैद्धान्तिक उपायों द्वारा भी हरित गृह प्रभाव को पूर्णतया तो समाप्त नहीं किया जा सकता है लेकिन इसमें कमी अवश्य की जा सकती है जो कि निम्न प्रकार हैं –
- वृक्षारोपण अधिक से अधिक किया जाना चाहिए जिससे हरित आवरण बढ़ सके।
- जनसंख्या वृद्धि को रोका जाना चाहिए।
- जीवाष्म ईंधन के स्थान पर सौर ऊर्जा, पवन ऊर्जा एवं ज्वारीय ऊर्जा के उपयोग में वृद्धि की जानी चाहिए।
- सोलर ऊर्जा एवं गोबर गैस संयंत्र को बढ़ावा दिया जाना चाहिए।
- स्वचालित वाहनों में पेट्रोल तथा डीजल के स्थान पर सी.एन.जी. एवं एल.पी.जी. आदि का प्रयोग किया जाना सुनिश्चित हो।
- पशुपालन अधिकतम होना चाहिए।
- क्लोरोफ्लोरोकार्बन पर प्रतिबन्ध हो तथा इसके उपभोक्ता देशों पर भी कड़ी नजर रखी जाये।
- जन जागरूकता के द्वारा जन सामान्य को औपचारिक तथा अनौपचारिक शिक्षा द्वारा हरित गृह प्रभाव के कारण होने वाली हानियों एवं दुष्परिणामों से अवगत कराया जाना चाहिए।
- वनों के विनाश को रोकना चाहिए।
- औद्योगिक इकाइयों तथा स्वचालित वाहनों से निकलने वाली ग्रीन गैसों को वातावरण में छोड़े जाने से रोकना चाहिए।
- यातायात के व्यक्तिगत साधनों का प्रयोग कम करना चाहिए तथा इसके स्थान पर साईकिल तथा जनसाधारण के यातायात के साधन काम में लेने चाहिए।
- कार पूल का प्रयोग करना चाहिए अर्थात् पास – पास रहने वाले एक ही विभाग के 3 – 4 कर्मचारी एक ही कार का प्रयोग कर सकते हैं।
उपर्युक्त उपायों के नहीं किए जाने पर मानव जाति ही नहीं अपितु सम्पूर्ण जीवमण्डल के लिए खतरा उत्पन्न हो जाएगा।
अम्ल वर्षा:
वायुमण्डल में उपस्थित कार्बन डाइऑक्साइड (CO2) की जल से क्रिया के कारण कार्बोनिक अम्ल (H2CO3) बनता है जिसके आयनन से प्राप्त H+ आयनों के कारण वर्षा जल की pH 5.6 से 6.0 के मध्य होती है। वायुमण्डल में उपस्थित सल्फर तथा नाइट्रोजन के ऑक्साइड जल में घुलकर अम्लीय बूंदों की रचना करते हैं। अम्लीय बूंदों का वर्षा के रूप में पृथ्वी पर आना अम्ल वर्षा कहलाता है।
H2O (l) + CO2 (g) → H2CO3 (aq)
H2CO3 (aq) + H+ (aq) + HCO3– (aq)
जब वर्षा जल की pH 5.6 से कम हो जाती है, तो इसे ‘अम्ल वर्षा’ कहते हैं।
अम्ल वर्षा का कारण – नाइट्रोजन तथा सल्फर के ऑक्साइड जो कि अम्लीय होते हैं, वायुमण्डल में ठोस कणों के साथ हवा में बहकर अन्त में धरती पर ठोस कणों के रूप में अथवा जल में द्रव रूप में कुहासे से या हिम की भाँति निक्षेपित होते हैं। मानवीय क्रियाकलापों से वातावरण में नाइट्रोजन तथा सल्फर के ऑक्साइड उत्सर्जित होते हैं। जीवाश्म ईंधन (जैसे – कोयला, शक्ति संयंत्रों, भट्टियों तथा मोटर इंजनों में डीजल तथा पेट्रोल (जिसमें सल्फर तथा नाइट्रोजन युक्त पदार्थ होते हैं) के दहन से सल्फर डाइऑक्साइड (SO2) तथा नाइट्रोजन के ऑक्साइड (NO2) उत्पन्न होते हैं। प्रदूषित वायु में उपस्थित कणिकीय द्रव्य ऑक्सीकरण को उत्प्रेरित करते हैं। अतः SO2 तथा NO2 का ऑक्सीकरण होता है तथा प्राप्त उत्पाद जल के साथ अभिक्रिया करके H2SO4 तथा HNO3 बनाते हैं जिनको अम्ल वर्षा में प्रमुख योगदान होता है।
2SO2 (g) + O2 (g) + 2H2O (l) → 2H2SO4 (aq)
NO + O3 → NO2O2
4NO2 (g) + O2 (g) + 2H2O (l) → 4HNO3 (aq)
इसमें अमोनियम लवण भी बनते हैं जो वायुमण्डलीय धुंध (एरोसॉल के सूक्ष्म कण) के रूप में दिखाई देते हैं। वर्षा की बूंदों में ऑक्साइड तथा अमोनियम लवणों के एरोसॉल कणों का नम निक्षेपण होता है।
अम्ल वर्षा के दुष्प्रभाव –
(1) अम्ल वर्षा कृषि तथा पेड़-पौधों आदि के लिए हानिकारक होती है, क्योंकि यह इनकी वृद्धि के लिए आवश्यक पोषक तत्वों (Ca, K, Fe, Mn) को घोलकर पृथक् कर देती है। जिससे मृदा की उर्वरा शक्ति कम होकर पेड़ – पौधों की वृद्धि में गिरावट होती है तथा इससे मृदा की अम्लीयता भी बढ़ती है।
(2) यह मनुष्यों तथा जानवरों में श्वसन में अवरोध पैदा करती है।
(3) जब अम्ल वर्षा का जल सतही जल के साथ बहकर नदी तथा झीलों तक पहुँचता है, तो जलीय पौधों एवं जन्तुओं के जीवन को प्रभावित करता है, इससे मछलियाँ तथा अन्य जीव मर जाते हैं।
(4) अम्ल वर्षा के कारण जल के पाइपों का संक्षारण होता है, जिससे आयरन, लेड, कॉपर आदि धातुएँ घुलकर पेयजल में पहुँच जाती हैं जो कि स्वास्थ्य के लिए हानिकारक है।
(5) यह पत्थर एवं धातुओं से बनी संरचनाओं तथा भवनों आदि को नष्ट करती है।
(6) हमारे देश में ताजमहल जैसी ऐतिहासिक इमारतें भी इससे प्रभावित हो रही हैं; क्योंकि सल्फ्यूरिक अम्ल तथा नाइट्रिक अम्ल दोनों ही संगमरमर को घोलकर क्रमशः CaSO4 तथा Ca(NO3)2 बनाते हैं।
CaCO3 + H2SO4 → CaSO4 + CO2+ H2O
CaCO3 + 2HNO3 → Ca(NO3)2 + CO2 + H2O
ये लवण जल के साथ धीरे – धीरे बह जाते हैं अतः इन स्मारकों का धीरे – धीरे क्षरण होता जा रहा है।
(7) अम्ल वर्षा से सड़कों तथा रेलमार्गों पर बने पुल कमजोर हो जाते हैं।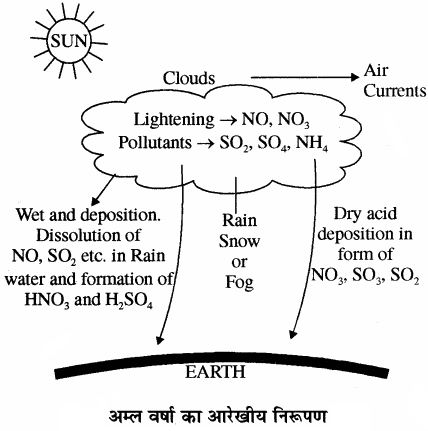
अम्ल वर्षा को कम करना – निम्नलिखित उपायों द्वारा अम्ल वर्षा को कम किया जा सकता है –
- शक्ति संयंत्रों तथा उद्योगों में सल्फर की कम मात्रा वाला ईंधन काम में लेना चाहिए।
- कोयले के स्थान पर प्राकृतिक गैस का प्रयोग करना चाहिए।
- उत्प्रेरकीय परिवर्तक युक्त गाड़ियों का प्रयोग करना चाहिए ताकि वायुमण्डल में उत्सर्जित धूम्र का प्रभाव कम हो सके। उत्प्रेरकीय परिवर्तक में सिरेमिक का मधुकोश होता है जिस पर Pd, Pt तथा Rh जैसी दुर्लभ धातुओं की परत चढ़ी होती है। गाड़ी (कार) से उत्सर्जित गैसें जिसमें बिना जला ईंधन, CO तथा NOx होते हैं जब 573 K ताप पर उत्प्रेरकीय परिवर्तक में से गुजरती है तो यह इन्हें CO2 तथा N2 में परिवर्तित कर देता है।
अम्ल वर्षा से बचाव –
अम्ल वर्षा से बचाव के उपाय निम्नलिखित हैं –
- अम्ल वर्षा के बाद इमारत को सामान्य जल से धोना।
- एन्टी अम्ल पदार्थ का छिड़काव करना।
- कम क्षेत्रफल वाले स्थान को प्लास्टिक से ढकना।
- अम्ल वर्षा के बाद शुष्क हवा बहाना।
- अम्ल वर्षा के बाद मृदा में क्षारीयता बढ़ाने वाले पदार्थ, जैसे चूना पत्थर डालना।
कणिकीय प्रदूषक –
वायु में निलंबित सूक्ष्म ठोस कण या द्रवीय बूंद कणिकीय प्रदूषक हैं। ये मोटर वाहनों के उत्सर्जन, आग के धूम्र, धूलकण एवं उद्योगों की राख होते हैं। ये कणिकाएँ जीवित (सजीव) तथा निर्जीव दोनों प्रकार की हो सकती हैं। जीवाणु, कवक, फफूद तथा शैवाल आदि जीवित कणिकाओं के उदाहरण हैं। जबकि धूम, धूल, कोहरा तथा धूम्र निर्जीव कणिकाएँ हैं। वायु में पाए। जाने वाले कुछ कवक मनुष्य में एलर्जी उत्पन्न करते हैं तथा ये पौधों में रोग भी उत्पन्न कर सकते हैं।
कणिकाओं का वर्गीकरण – कणिकाओं के आकार तथा उनकी प्रकृति के आधार पर इन्हें चार भागों में वर्गीकृत किया जाता है –
(1) धूम – धूम कणिकाओं में ठोस तथा ठोस – द्रव कणों का मिश्रण होता है, जो कि कार्बनिक पदार्थों के दहन से उत्पन्न होते हैं, जैसे – सिगरेट का धुआँ, जीवाश्म ईंधन के दहन से प्राप्त धूम्र, गंदगी का ढेर, सूखी पत्तियाँ तथा तेल – धूम्र इत्यादि।
(2) धूल – धूल में बारीक ठोस कण (व्यास 1 – 4 µm से अधिक) होते हैं, जो ठोस पदार्थों के पीसने, कुचलने तथा आरोपण से बनते हैं। विस्फोट से प्राप्त बालू, लकड़ी के कार्य से प्राप्त बुरादा, कोयले का बुरादा, कारखानों से उड़ने वाली राख, सीमेन्ट तथा धुएँ के गुबार इत्यादि इस प्रकार के कणिकीय उत्सर्जन के कुछ प्रारूपिक उदाहरण हैं।
(3) कोहरा – फैले हुए द्रव – कणों एवं वाष्प के हवा में संघनन से कोहरा उत्पन्न होता है। जैसे – सल्फ्यूरिक अम्ल का कोहरा तथा शाकनाशी व कीटनाशी, जो अपने लक्ष्य पर न जाकर हवा से गमन करते हैं तथा कोहरा बनाते हैं।
(4) धूम् – धूम्र सामान्यतया ऊर्ध्वपातन, आसवन, क्वथन एवं अन्य रासायनिक अभिक्रियाओं के दौरान प्राप्त वाष्प के संघनन के कारण बनते हैं। प्रायः कार्बनिक विलायक, धातुएँ तथा धात्विक ऑक्साइड धूम्र कणों का निर्माण करते हैं।
कणिकीय प्रदूषकों का प्रभाव – कणिकीय प्रदूषकों का प्रभाव मुख्यतः उनके कणों के आकार पर निर्भर करता है। हवा द्वारा उत्पन्न कण, जैसे – धूल, धूम, कोहरा आदि मनुष्य के स्वास्थ्य के लिए हानिकारक होते हैं। 5 माइक्रोन से बड़े कणिकीय प्रदूषक नासिकाद्वार में एकत्रित हो जाते हैं, जबकि 1.0 माइक्रोन के कण फेफड़ों में आसानी से प्रवेश कर जाते हैं। वाहनों द्वारा उत्सर्जित लेड मुख्य वायु – प्रदूषक होता है। भारतीय शहरों में लेडयुक्त पेट्रोल वायुजनित लेड – उत्सर्जन का प्राथमिक स्रोत है। लेडविहीन (सीसारहित) पेट्रोल का उपयोग करके इस समस्या पर नियंत्रण किया जा सकता है। लेड, लाल रक्त कणिकाओं के विकास एवं उनके परिपक्व होने में बाधा उत्पन्न करता है।
धूम कोहरा या स्मॉग –
स्मॉग एक कोलॉइडी तंत्र है जिसका निर्माण वायुमण्डल में । कोहरा तथा धूम से मिलकर होता है। (स्मोग = स्मोक + फोग) यह वायु प्रदूषण का एक प्रमुख उदाहरण है जो कि विश्व के अनेक शहरों में होता है जहाँ तापमान कम रहता है।
वर्गीकरण – स्मॉग को उसके बनने तथा संरचना के आधार पर दो वर्गों में वर्गीकृत किया जाता है –
(1) अपचायक स्मॉग – इसे सामान्य स्मॉग भी कहते हैं। यह शीतल (ठण्डी) तथा नम जलवायु में उत्पन्न होता है। इसका कारण वायुमण्डल में उपस्थित SO2 गैस है। ईंधन तथा वाहनों में दहन से वायुमण्डल में SO2 गैस उत्सर्जित होती है जो कि धूम तथा कोहरे के साथ मिलकर इसका निर्माण करती है अतः अपचायक स्मॉग धूम, कोहरा तथा SO2 का मिश्रण है। अपचायक स्मॉग का निर्माण सूर्योदय से पूर्व होता है। सूर्योदय के पश्चात् कुछ समय तक इसका प्रभाव बढ़ता जाता है; क्योंकि सूर्य के प्रकाश में SO2, SO3 में ऑक्सीकृत हो जाती है। SO3 जल से क्रिया करके H2SO4 का ऐरोसॉल बनाती है जो कि धुएँ के कार्बन कणों पर संघनित होकर स्मॉग का निर्माण करती है।
2SO2 + O2 → 2SO3
SO3 + H2O → H2SO4
रासायनिक रूप से यह एक अपचायक मिश्रण है।
(2) ऑक्सीकारक स्मॉग – इसे प्रकाश रासायनिक स्मॉग भी कहते हैं। यह गर्म (उष्ण), शुष्क, स्वच्छ तथा धूप युक्त जलवायु में बनता है। मोटरवाहनों तथा कारखानों से उत्सर्जित नाइट्रोजन के ऑक्साइडों तथा हाइड्रोकार्बनों पर सूर्य के प्रकाश की क्रिया से इसका निर्माण होता है। प्रकाश रासायनिक स्मॉग में ऑक्सीकारक पदार्थों की सान्द्रता उच्च होती है इसलिए इसे ऑक्सीकारक स्मॉग भी कहा जाता है।
प्रकाश रासायनिक धूम कोहरे का निर्माण – जब स्वचालित वाहनों तथा कारखानों में जीवाश्म ईंधनों का दहन होता है, तब पृथ्वी के वातावरण में कई प्रदूषकों का उत्सर्जन होता है। इनमें हाइड्रोकार्बन (अदहित ईंधन) तथा नाइट्रिक ऑक्साइड (NO) मुख्य हैं। जब इन प्रदूषकों का स्तर बहुत अधिक हो जाता है, तो सूर्य के प्रकाश से इनकी क्रिया के कारण श्रृंखला अभिक्रिया होती है, जिससे NO, नाइट्रोजन डाइऑक्साइड (NO2) में परिवर्तित हो जाती है।
2NO(g) + O2(g) → 2NO2(g)
यह सूर्य के प्रकाश से ऊर्जा ग्रहण करके पुनः नाइट्रिक ऑक्साइड तथा मुक्त ऑक्सीजन परमाणु में विघटित हो जाती है।![]()
ऑक्सीजन परमाणु के अत्यधिक क्रियाशील होने के कारण यह O2 के साथ संयुक्त होकर उसे ओजोन में परिवर्तित कर देता है।
O(g) + O2(g) → O3(g)
इस प्रकार प्राप्त ओजोन पूर्व में प्राप्त NO से तेजी से क्रिया करके पुनः NO2 बनाती है।
NO(g) + O3(g) → NO2(g) +O2(g)
यह एक भूरी गैस होती है, जिसका उच्च स्तर धुंध का कारण हो सकता है। NO2 तथा O3 दोनों ही प्रबल ऑक्सीकारक हैं अतः ये प्रदूषित वायु में उपस्थित अदहित हाइड्रोकार्बन जैसे मेथेन इत्यादि से क्रिया करके कई हानिकारक कार्बनिक यौगिकों जैसे फॉर्मेल्डिहाइड (HCHO), एक्रोलीन (CH2 = CH – CHO) तथा परॉक्सी ऐसीटिल नाइट्रेट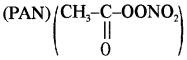
(द्वितीयक प्रदूषक) का निर्माण करते हैं।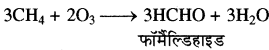
प्रकाश रासायनिक धूम कोहरे के प्रभाव –
- प्रकाश रासायनिक धूम कोहरे के सामान्य घटक ओजोन, नाइट्रिक ऑक्साइड, एक्रोलीन, फार्मेल्डिहाइड एवं परॉक्सीऐसीटिल नाइट्रेट (PAN) हैं।
- इसके कारण गंभीर स्वास्थ्य समस्याएँ उत्पन्न होती हैं। जैसे O3 तथा NO नाक एवं गले में जलन पैदा करते हैं।
- ओजोन तथा PAN आँखों में बहुत अधिक जलन उत्पन्न करते हैं।
- ओजोन तथा नाइट्रिक ऑक्साइड की उच्च सान्द्रता से सिरदर्द, छाती में दर्द, गले का शुष्क होना, खाँसी तथा श्वास लेने में तकलीफ जैसी समस्याएँ उत्पन्न होती हैं।
- प्रकाश रासायनिक धूम कोहरे से रबर में दरार उत्पन्न हो जाती है।
- यह धातुओं, पत्थरों, भवन निर्माण सामग्री तथा पेन्ट की हुई सतहों का संक्षारण करता है।
- इससे पौधों पर भी हानिकारक प्रभाव होता है।
प्रकाश रासायनिक धूम कोहरे का नियंत्रण –
प्रकाश रासायनिक धूम – कोहरे को नियंत्रित करने के लिए कई तकनीकों का प्रयोग किया जाता है। यदि प्रकाश रासायनिक धूम – कोहरे के लिए जिम्मेदार प्राथमिक पूर्वगामी, जैसे – NO2 तथा हाइड्रोकार्बन को नियंत्रित कर लिया जाए तो द्वितीयक पूर्वगामी जैसे – ओजोन, PAN तथा प्रकाश रासायनिक धूम – कोहरा स्वतः ही कम हो जाएगा। स्वचालित वाहनों में उत्प्रेरित परिवर्तक के प्रयोग से वायुमण्डल में नाइट्रोजन के ऑक्साइड तथा हाइड्रोकार्बन का उत्सर्जन बहुत कम होता है। क्वेरकस पाईनस, पायरस, विटिस तथा जुनीपेरस जैसे पौधे नाइट्रोजन ऑक्साइडों का उपापचयन करते हैं अतः इनके रोपण से भी प्रकाश रासायनिक धूम कोहरे के निर्माण में कमी लायी जा सकती है।
समतापमंडलीय प्रदूषण:
ओजोन का विरचन एवं विघटन –
ऊपरी समताप – मण्डल (समुद्र तल से 10 – 50 km ऊपर तक का क्षेत्रफल) में ओजोन प्रचुर मात्रा में होती है। इसके अतिरिक्त N2, O2 तथा सूक्ष्म मात्रा में जल वाष्प भी पायी जाती है। ओजोन सूर्य से आने वाली पराबैंगनी विकिरणों के 99.5 प्रतिशत भाग को रोककर हमें इन हानिकारक विकिरणों से बचाती है। इन विकिरणों से त्वचा – कैंसर (मेलेनोमा) होता है। अतः ओजोन – कवच को बचाए रखना आवश्यक है। समतापमण्डल में पराबैंगनी विकिरणों की ऑक्सीजन से क्रिया द्वारा ओजोन का निर्माण होता है। पराबैंगनी विकिरण आण्विक ऑक्सीजन को मुक्त ऑक्सीजन (O) परमाणुओं में विखण्डित कर देते हैं। जो कि आण्विक ऑक्सीजन से संयुक्त होकर ओजोन बनाते हैं।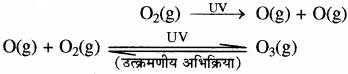
ओजोन ऊष्मागतिकीय रूप से अस्थायी होती है एवं यह आण्विक ऑक्सीजन में विघटित हो जाती है। इस प्रकार ओजोन के निर्माण एवं विघटन के मध्य एक गतिक साम्य स्थापित हो जाता है। अभी हाल ही के वर्षों में समतापमण्डल में उपस्थित कुछ रसायनों के कारण ओजोन की इस सुरक्षा – परत का क्षय होना प्रारम्भ हो गया है। ओजोन परत के इस क्षय का मुख्य कारण क्लोरोफ्लोरोकार्बन (फ्रेऑन) (CFCs) का उत्सर्जन है। फ्रेऑन अक्रिय, अज्वलनशील तथा अविषाक्त पदार्थ हैं, अतः इन्हें रेफ्रिजरेटर, एयर – कंडीशनर, प्लास्टिक फोम के निर्माण में एवं इलेक्ट्रॉनिक उद्योग में कम्प्यूटर के पुर्षों की सफाई करने में प्रयुक्त किया जाता है। सामान्यतः ताप तथा दाब की परिस्थितियों में भूमध्य रेखा के ऊपर ओजोन की सांद्रता 0.29 cm और ध्रुवों पर यह 0.40 cm तक पायी जाती है।
वायुमण्डल में एक बार फ्रेऑन के उत्सर्जित होने पर ये वायुमण्डल की अन्य गैसों के साथ मिलकर सीधे समतापमण्डल में पहुँच जाते हैं। समतापमण्डल में ये शक्तिशाली पराबैंगनी विकिरणों द्वारा विघटित होकर क्लोरीन मुक्त मूलक बनाते हैं।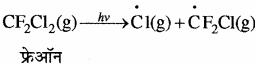
क्लोरीन मुक्त मूलक समतापमण्डल में स्थित ओजोन से अभिक्रिया करके क्लोरीन मोनोऑक्साइड मूलक ((dot { C } )lO) तथा आण्विक ऑक्सीजन बनाते हैं।![]()
क्लोरीन मोनोऑक्साइड मूलक परमाण्वीय ऑक्सीजन के साथ अभिक्रिया करके अधिक क्लोरीन मूलक उत्पन्न करता है।![]()
इस प्रकार क्लोरीन मूलक लगातार बनते रहते हैं तथा ओजोन को विखण्डित करते रहते हैं। अतः CFC समतापमण्डल में क्लोरीन मूलकों को उत्पन्न करने वाले एवं ओजोन परत को क्षति पहुँचाने वाले परिवहनीय कारक हैं। ओजोन परत के क्षय के कारणों को खोजने के लिए शेरवुड रोलेण्ड मारियो मेलिना एवं पॉल क्रट्जन को सन् 1945 में रसायन शास्त्र के क्षेत्र में नोबल पुरस्कार से सम्मानित किया गया।
ओजोन छिद्र –
सन् 1980 में वायुमण्डलीय वैज्ञानिकों ने अंटार्कटिका पर कार्य करते हुए दक्षिणी ध्रुव के ऊपर ओजोन परत के क्षय के बारे में बताया जिसे सामान्य रूप से ‘ओजोन छिद्र’ कहा जाता है। गरमी में नाइट्रोजन डाइऑक्साइड तथा मेथेन क्रमशः क्लोरीन मोनोऑक्साइड तथा क्लोरीन परमाणुओं से अभिक्रिया करके क्लोरीन सिंक बनाते हैं, जो ओजोन – क्षय को काफी हद तक रोकता है।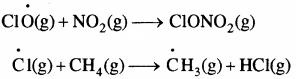
सर्दी के मौसम में अंटार्कटिका के ऊपर विशेष प्रकार के बादल बनते हैं जिन्हें ध्रुवीय समतापमण्डलीय बादल कहते हैं। ये बादल एक प्रकार की सतह प्रदान करते हैं जिस पर क्लोरीन नाइट्रेट जलअपघटित होकर हाइपोक्लोरस अम्ल बनाता है तथा उपरोक्त अभिक्रिया में उत्पन्न हाइड्रोजन क्लोराइड भी क्लोरीन नाइट्रेट से क्रिया करके आण्विक क्लोरीन देता है।
ClONO2 (g) + H2O (g) → HOCl (g) + HNO3 (g)
ClONO2 (g) + HCl (g) → Cl2 (g) + HNO3 (g)
बसंत ऋतु में जब सूर्य का प्रकाश अंटार्कटिका पर आता है तो सूर्य की गर्मी से बादल विखण्डित हो जाते हैं तथा सूर्य के प्रकाश से HOCl तथा Cl2 का भी अपघटन हो जाता है।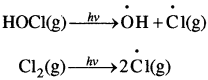
इस प्रकार उत्पन्न क्लोरीन मूलक, ओजोन क्षय के लिए श्रृंखला अभिक्रिया प्रारम्भ कर देते हैं।
उपरोक्त अभिक्रियाओं को सम्मिलित रूप से इस प्रकार लिखा जा सकता है –![]()
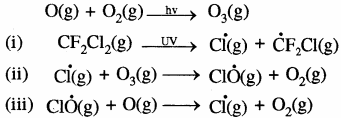
ओजोन परत के क्षय के प्रभाव:
ओजोन परत के क्षय के कारण अधिकाधिक पराबैंगनी विकिरण क्षोभमण्डल में छनित होते हैं, जिनसे त्वचा का जीर्णन, मोतियाबिंद, सनबर्न, त्वचा – कैंसर जैसी बीमारियाँ होती हैं तथा इससे पादपप्लवकों की मृत्यु तथा मत्स्य उत्पादन में कमी होती है। पौधों के प्रोटीन, पराबैंगनी विकिरणों से आसानी से प्रभावित हो जाते हैं, जिससे कोशिकाओं में हानिकारक उत्परिवर्तन होता है। इसके कारण पत्तियों के रंध्रों से जल का वाष्पीकरण बढ़ जाता है, जिससे मिट्टी की नमी कम हो जाती है। बढ़े हुए पराबैंगनी विकिरण रंगों एवं रेशों को भी हानि पहुंचाते हैं, जिससे रंग जल्दी हल्के हो जाते हैं।पराबैंगनी विकिरणों से शरीर के सम्पूर्ण प्रतिरोधी तंत्र की कार्यक्षमता में गिरावट आ जाती है। इनसे शिशुओं में भी विकृतियाँ उत्पन्न हो जाती हैं। ये विकिरण प्रकाश संश्लेषण की क्रिया को भी कम करते हैं। इनसे जैविक तत्त्वों के आनुवंशिक घटक न्यूक्लिक अम्ल को भी क्षति पहुँचती है तथा जीवन की खाद्य श्रृंखलाएँ अनियंत्रित हो जाती हैं। इस प्रकार इनसे सम्पूर्ण पारिस्थितिकी तंत्र पर विनाशकारी प्रभाव पड़ता है।
वायु प्रदूषण का नियन्त्रण –
निम्नलिखित उपायों द्वारा वायु प्रदूषण को काफी हद तक कम किया जा सकता है –
- वायु प्रदूषण का सार्थक नियन्त्रण ‘हरित क्रान्ति’ द्वारा सम्भव है।
- औद्योगिक चिमनियों से निकलने वाली गैसों को कार्बन से मुक्त करके वायुमण्डल में छोड़ा जाना चाहिए।
- सीमित क्षेत्र में ही विशेष प्रकार के प्रदूषण रहित उद्योगों को स्थापित किया जाना चाहिए।
- मोटर वाहनों में सीसारहित पेट्रोल का प्रयोग किया जाना चाहिए।
- वाहनों में उत्प्रेरकीय कन्वर्टर’ लगाकर प्रदूषण को कम करना चाहिए।
- C.N.G. गैसयुक्त वाहनों को ही चलने की अनुमति प्रदान की जानी चाहिए।
- ईंधन के रूप में गोबर गैस, बायो गैस इत्यादि का प्रयोग किया जाना चाहिए।
- यथासंभव जीवाश्म ईंधन के स्थान पर सौर ऊर्जा द्वारा चलित वाहनों का प्रयोग किया जाना चाहिए।
- कूड़ा और जैव-क्षय के पदार्थों को खुली वायु में नहीं छोड़ा जाना चाहिए।
- मानवीय – जागरूकता द्वारा भी वायु – प्रदूषण को कम किया जा सकता है। जैसे – लाल बत्ती संकेतक पर खड़े हजारों वाहन यदि इंजन को कुछ समय के लिए बन्द कर दें तो काफी मात्रा में वायु प्रदूषण कम हो सकता है।
प्रश्न 26.
हरित रसायन क्या है तथा प्रदूषण घटाने में इसके योगदान का वर्णन कीजिये।
उत्तर:
हरित रसायन:
पर्यावरण प्रदूषण को नियंत्रित करने के लिए 1990 के दशक में एक सिद्धान्त प्रतिपादित किया गया जिसे हरित रसायन के नाम से जाना जाता है। इसके अनुसार उन प्रक्रियाओं, प्रणालियों एवं उत्पादों को विकसित करने पर जोर दिया जाना चाहिए जो हानिकारक पदार्थों के उपयोग और उत्पादन को यथासंभव कम कर दे या रोक दे, जिससे विषैले पदार्थ वायुमण्डल, जल या भूमि में विसरित ना हो तथा पर्यावरण को प्रदूषित ना कर सके। अतः रसायन विज्ञान तथा विज्ञान की अन्य शाखाओं के उन सिद्धान्तों का ज्ञान, जिनके प्रयोग से पर्यावरण के दुष्प्रभावों को कम किया जा सकता है, उसे ‘हरित रसायन’ कहते हैं। हरित रसायन के अनुसार औद्योगिक जगत में, प्रयोग शालाओं में तथा अनुसंधान संस्थाओं में उन अभिकर्मकों, आरम्भिक पदार्थों, विलायकों आदि का प्रयोग किया जाना चाहिए जो मानव समाज एवं पर्यावरण के लिए हानिकारक न हो या कम हो तथा ये कम से कम अपशिष्ट या न्यूनतम अपशिष्ट उत्पन्न करे।
वस्त्रों की धुलाई में प्रयुक्त होने वाले अपमार्जकों को एंजाइमों द्वारा समाप्त किया जाए। वाहनों में उपयोग में लिए जाने वाले ईंधन के धुएँ से वायु प्रदूषण होता है। अतः वैज्ञानिक खोजों से हाइड्रोजन, बायोडीजल तथा ईंधन सेल से चलने वाले वाहनों को विकसित करने का प्रयास किया जा रहा है। कुछ ऐसे जलीय एवं अजलीय विलायक तैयार किए जा रहे हैं जो मानव स्वास्थ्य के लिए हानिकारक नहीं है और न ही पर्यावरण को प्रदूषित करते हैं। जल कीउच्च विशिष्ट ऊष्मा तथा कम वाष्पशीलता के कारण इसे संश्लेषित अभिक्रियाओं में माध्यम के रूप में प्रयुक्त किया जा सकता है। जल सस्ता, अज्वलनशील एवं अकैंसरजन्य माध्यम है।
कुछ ऐसे उपकरण तथा प्रक्रियाओं का विकास किया जा रहा है जो अपशिष्टों को औद्योगिक रसायनों तथा ईंधन आदि में बदल देता है। कृषि रसायन की नवीन विधियों के अनुसार सायनाइड जैसे विषैले पदार्थों के उपयोग की आवश्यकता ही नहीं होगी। फ्रिओन्स (क्लोरोफ्लोरोकार्बन) के स्थान पर द्रव नाइट्रोजन, द्रव कार्बन डाइऑक्साइड आदि का प्रयोग किया जा रहा है। रासायनिक अभिक्रियाओं को पराबैंगनी प्रकाश ध्वनि तरंगों एवं सूक्ष्म तरंगों आदि की उपस्थिति में करवाए जाने का प्रयास किया जा रहा है। इसी तरह उत्प्रेरकों को काम में लेते हुए भी अभिक्रिया करवायी जा सकती है। कुछ देशों में सल्फर डाइ ऑक्साइड को तप्त कोल विधि अथवा चूने के पत्थर से परिवर्तित कर दिया जाता है, अतः इससे होने वाला प्रदूषण कम हो जाता है।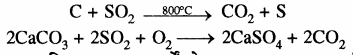
अतः हरित रसायन पदार्थों के उत्पादन का प्रक्रम है जो पर्यावरण में न्यूनतम प्रदूषण उत्पन्न करता है। सारांशतः यह कहा जा सकता है कि विकास कार्यों के साथ – साथ वर्तमान ज्ञान का रासायनिक हानि को कम करने के लिए उपयोग में लाना ही हरित रसायन का मूल आधार है।
दैनिक जीवन में हरित रसायन – दैनिक जीवन में हरित रसायन को निम्नलिखित उदाहरणों द्वारा समझा जा सकता है –
(1) कपड़ों की निर्जल धुलाई में –
प्रारम्भ में निर्जल धुलाई के लिए टेट्राक्लोरोएथीन (CCl2 = CCl2) का उपयोग किया जाता था लेकिन यह भू – जल को प्रदूषित कर देता है तथा यह एक संभावित कैंसरजन्य भी है। अतः आजकल धुलाई में इसके स्थान पर उपयुक्त अपमार्जक के साथ द्रव CO2 को प्रयुक्त किया जाता है। हैलोजेनीकृत विलायक का द्रव CO2 से प्रतिस्थापन भू – जल के लिए कम हानिकारक होता है। आजकल लॉन्ड्री में कपड़ों के विरंजन के लिए हाइड्रोजन परॉक्साइड का उपयोग किया जाता है, जिससे अच्छे परिणाम प्राप्त होते हैं तथा इसमें जल का उपयोग भी कम होता है।
(2) पेपर का विरंजन –
पहले पेपर के विरंजन के लिए क्लोरीन गैस उपयोग में लेते थे। आजकल उत्प्रेरक की उपस्थिति में हाइड्रोजन परॉक्साइड को विरंजन के लिए प्रयोग में लाया जाता है, जिससे विरंजन की दर बढ़ जाती है।
(3) रसायनों का संश्लेषण –
रासायनिक उत्प्रेरकों की उपस्थिति में जलीय विलयन में एथीन के ऑक्सीकरण से लगभग 90% एथेनैल प्राप्त होता है। यह एथेनैल बनाने की व्यापारिक विधि है।![]()
संक्षेप में, हरित रसायन एक कम लागत का उपागम है, जो कम पदार्थ, कम ऊर्जा-उपभोग तथा कम अपशिष्ट जनन से सम्बन्धित है।
All Chapter RBSE Solutions For Class 11 Chemistry Hindi Medium
—————————————————————————–
All Subject RBSE Solutions For Class 11 Hindi Medium
*************************************************
————————————————————
All Chapter RBSE Solutions For Class 11 Chemistry Hindi Medium
All Subject RBSE Solutions For Class 11 Hindi Medium
Remark:
हम उम्मीद रखते है कि यह RBSE Class 11 chemistry Solutions in Hindi आपकी स्टडी में उपयोगी साबित हुए होंगे | अगर आप लोगो को इससे रिलेटेड कोई भी किसी भी प्रकार का डॉउट हो तो कमेंट बॉक्स में कमेंट करके पूंछ सकते है |
यदि इन solutions से आपको हेल्प मिली हो तो आप इन्हे अपने Classmates & Friends के साथ शेयर कर सकते है और HindiLearning.in को सोशल मीडिया में शेयर कर सकते है, जिससे हमारा मोटिवेशन बढ़ेगा और हम आप लोगो के लिए ऐसे ही और मैटेरियल अपलोड कर पाएंगे |
आपके भविष्य के लिए शुभकामनाएं!!