इस unit cell में घन के आठों कोनों पर आठ परमाणु होते है। यह यूनिट सेल एक परमाणु की बनी होती है।
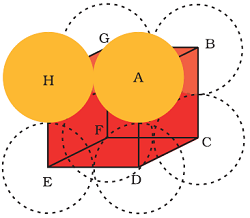
एक सरल घनीय जालक में केवल घन के कोनों पर परमाणु उपस्थित होते हैं।
मान लिया कि घन के एक भुजा की लम्बाई =a तथा प्रत्येक कण की त्रिज्या r है।
चूँकि घन के किनारों पर कण एक दूसरे के संपर्क में होते हैं,
अत: a=2r
घनीय एकक कोष्ठिका का आयतन =a3=(2r)3=8r3
चूँकि सरल घनीय एकक कोष्ठिका में केवल 1 परमाणु होता है। अत: परमाणु द्वारा भरे हुए स्थान का आयतन =43prr3
अत: संकुलन क्षमता

=4/3πr38r3×100
=π6×100
=52.36%=52.4%
अत:
(a) hcp और ccp संरचनाओं में संकुलन क्षमता (packing efficiency) = 74%
(b) अंत: केन्द्रित घनीय (bcc) संरचनाओं में संकुलन क्षमता (packing efficiency) = 68%
(c) तथा सरल घनीय जालक (simple cubic lattice) में संकुलन क्षमता (packing efficiency) = 52.4%
अर्थात hcp और ccp संरचनाओं में संकुलन क्षमता (packing efficiency) अधिकतम होती है।
एकक कोष्ठिका विमा संबंधी गणनाएं :
Unit cell के dimension की सहायता से यूनिट सेल का आयतन निकाला जा सकता है।
मान लिया कि Cubic crystal (घनीय क्रिस्टल) के Unit cell (एकक कोष्ठिका) के
कोर की लम्बाई =a
पदार्थ का घनत्व (Density) =d (पदार्थ तथा एकक कोष्ठिका का घनत्व बराबर होता है।)
तथा मोलर द्र्वयमान (Molar Mass) =M है।
अत: Cubic Crystal (घनीय क्रिस्टल) के
Unit cell (एकक कोष्ठिका) का आयतन =a3
Unit cell (एकक कोष्ठिका) का द्र्व्यमान = एकक कोष्ठिका में परमाणु की संख्यां × एक परमाणु का द्रव्यमान
=z⋅m
(जहाँ z= एकक कोष्ठिका में उपस्थित परमाणुओं की संख्या
तथा m= एक परमाणु का द्रव्यमान)
एकक कोष्ठिका में उपस्थित एक परमाणु का द्रव्यमान
m=MNA
(जहाँ M= मोलर द्र्व्यमान तथा NA= एवोगाड्रो संख्या है।)
अत: एकक कोष्ठिका का घनत्व, d

⇒d=z⋅ma3
⇒d=z⋅Ma3⋅NA
⇒d=zMd3NA
अत: उपरोक्त सूत्र के पाँच पैरामीटरों, d, z, M, a तथा NA, में से किसी चार के ज्ञात रहने पर पाँचवें की गणना उपरोक्त सूत्र से, की जा सकती है।
FCC संरचना के लिए यूनिट सेल के किनारो की लम्बाई व परमाणु त्रिज्या के मध्य सम्बन्ध:
r = a/2√2
BCC संरचना के लिए यूनिट सेल के किनारों (कोर) की लम्बाई व परमाणु त्रिज्या के मध्य सम्बन्ध:
r = √3 . a/4










