हेलो स्टूडेंट्स, यहां हमने राजस्थान बोर्ड कक्षा 11वीं की भौतिक विज्ञान सॉल्यूशंस को दिया हैं। यह solutions स्टूडेंट के परीक्षा में बहुत सहायक होंगे | Student RBSE solutions for Class 11 Physics Chapter 13 ऊष्मागतिकी pdf Download करे| RBSE solutions for Class 11 Physics Chapter 13 ऊष्मागतिकी notes will help you.
Table of Contents
Rajasthan Board RBSE Class 11 Physics Chapter 13 ऊष्मागतिकी
RBSE Class 11 Physics Chapter 13 पाठ्य पुस्तक के प्रश्न एवं उत्तर
RBSE Class 11 Physics Chapter 13 अतिलघूत्तरात्मक प्रश्न
प्रश्न 1.
यदि दो निकाय A व B किसी तीसरे निकाय C से अलग-अलग ऊष्मीय साम्य अवस्था में हैं तो A व B क्या आपस में ऊष्मीय साम्य अवस्था में होंगे ?
उत्तर:
हाँ।
प्रश्न 2.
क्या ऊष्मागतिकी के प्रथम नियम से किसी क्रिया के होने की दिशा को ज्ञान हो सकता है?
उत्तर:
नहीं।
प्रश्न 3.
मेयर का सम्बन्ध लिखिये।
उत्तर:
Cp – Cv = R
जहाँ Cp = नियत दाब पर मोलरे विशिष्ट ऊष्मा, Cv = नियत आयतन पर मोलर विशिष्ट ऊष्मा व R = सार्वत्रिक गैस नियतांक है।
प्रश्न 4.
किसी आदर्श गैस के रुद्धोष्म प्रसार में P व V के मध्य सम्बन्ध लिखिये।
उत्तर:
PVγ = नियतांक, जहाँ γ = (left(frac{mathrm{C}_{mathrm{p}}}{mathrm{C}_{mathrm{v}}}right))
प्रश्न 5.
ऊष्मा इंजन की दक्षता की विमा क्या होती है?
उत्तर:
दक्षता विमाहीन है।
प्रश्न 6.
समदाबीय प्रक्रम में निकाय की अवस्था परिवर्तन से दाब में क्या परिवर्तन होता है?
उत्तर:
शून्य
प्रश्न 7.
क्या किसी गैस के ताप में वृद्धि बिना ऊष्मा दिये की जा सकती है?
उत्तर:
हाँ, रुद्धोष्म प्रक्रम में होती है।
प्रश्न 8.
ऊष्मागतिकी का शून्य नियम किस ऊष्मागतिकी चर को परिभाषित करता है?
उत्तर:
ताप
प्रश्न 9.
समतापीय व रुद्धोष्म प्रक्रम में किसी गैस की विशिष्ट ऊष्मा क्या होती है?
उत्तर:
समतापीय में अनन्त व रुद्धोष्म प्रक्रम में शून्य।
प्रश्न 10.
कार्नो चक्र किस प्रकार का प्रक्रम है?
उत्तर:
उत्क्रमणीय चक्रीय प्रक्रम।
प्रश्न 11.
कार्बो इंजन की दक्षता किस पर निर्भर करती है?
उत्तर:
स्रोत व सिंक के ताप पर
RBSE Class 11 Physics Chapter 13 लघूत्तरात्मक प्रश्न
प्रश्न 1.
“उत्क्रमणीयता एक आदर्श इंजन की कसौटी है।” उक्त कथन की व्याख्या कीजिये।
उत्तर:
उत्क्रमणीय प्रक्रम (Reversible Process) वह क्रिया है जिसको विपरीत क्रम में ठीक उन्हीं अवस्थाओं में सम्पन्न किया जा सके, जिनमें उसे सीधे क्रम में सम्पन्न किया गया था। सीधे प्रक्रम में कार्यकारी द्रव्य यदि ΔQ ऊष्मा अवशोषित करता है तथा ΔW कार्य करता है, तो विपरीत क्रम में कार्यकारी द्रव्य पर ΔW कार्य करने से ΔQ ऊष्मा प्राप्त हो जायेगी। ऐसे प्रक्रम को उत्क्रमणीय प्रक्रम कहते हैं।
उत्क्रमणीय प्रक्रम में भाग लेने वाले निकाय और परिवेश (surroundings) की अवस्था में कोई परिवर्तन नहीं होता है। उत्क्रमणीय प्रक्रम एक आदर्श प्रक्रम है एवं इसके लिए निम्न शर्तों की पालना आवश्यक है।
- चालन, संवहन तथा विकिरण से ऊर्जा की हानि नहीं होनी चाहिए।
- ऊर्जा की हानि करने वाले प्रभाव जैसे घर्षण, विद्युत प्रतिरोध, श्यानता आदि नहीं होने चाहिए।
- परिवर्तन बहुत धीमी गति से होने चाहिए।
- निकाय साम्यावस्था की स्थिति में अधिक विचलित नहीं होना चाहिए।
अतः हम कह सकते हैं कि उत्क्रमणीय प्रक्रम के लिए आवश्यक शर्तों की पालना, व्यवहार में असम्भव है या यूँ कहें कि उत्क्रमणीयता एक आदर्श इंजन की कसौटी है।
प्रश्न 2.
ऊष्मा इंजन की दक्षता की व्याख्या कीजिये।
उत्तर:
ऊष्मा इंजन की दक्षता-“एक चक्र में, इंजन द्वारा किये गये उपयोगी कार्य तथा कार्यकारी पदार्थ द्वारा स्रोत से प्राप्त की गयी ऊष्मा के अनुपात को इंजन की दक्षता कहते हैं। इसे η से व्यक्त करते हैं।
उदाहरणार्थ यदि किसी इंजन के कार्यकारी पदार्थ ने स्रोत से 100 जूल ऊष्मा लेकर 40 जूल के समान उपयोगी कार्य किया तो उसकी दक्षता![]()
कोई भी इंजन सम्पूर्ण ली गई ऊष्मा को पूर्ण रूप से कार्य में परिवर्तित नहीं कर सकता है। अर्थात् किसी भी इंजन की दक्षता 100% नहीं हो सकती है।
प्रश्न 3.
ऊष्मागतिकी क्या है? ऊष्मागतिकी के शून्यांकी नियम की व्याख्या कीजिये तथा इसके महत्व पर प्रकाश डालिये?
उत्तर:
ऊष्मागतिकी भौतिकी की वह शाखा है जिसमें ताप व ऊष्मा की अभिधारणाओं (Concepts) एवं ऊष्मीय ऊर्जा (Thermal Energy) का अन्य ऊर्जाओं में तथा अन्य ऊर्जाओं के ऊष्मीय ऊर्जा में रूपान्तरण का अध्ययन किया जाता है। ऊष्मागतिकी, ऊष्मा तथा यांत्रिक कार्य के पारस्परिक सम्बन्ध का भी वर्णन करती है।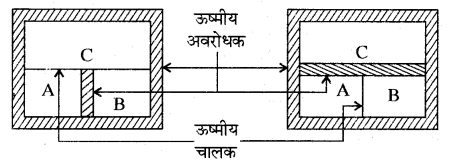
शून्यांकी नियम ऊष्मागतिकी को मूलभूत सिद्धान्त है एवं ताप को परिभाषित करता है। इसके अनुसार यदि दो निकाय A व B अलगअलग तीसरे निकाय से साथ तापीय संतुलन में हैं तो A तथा B निकाय भी आपस में तापीय संतुलन में होंगे।
प्रश्न 4.
एक निकाय की ऊष्मा, कार्य व आन्तरिक ऊर्जा की व्याख्या कीजिये।
उत्तर:
ऊष्मा (Heat)— यह दो निकायों के मध्य स्थानान्तरित होने वाली ऊर्जा है। जब किन्हीं दो निकायों के बीच ऊर्जा स्थानान्तरण निकायों के बीच तापान्तर के कारण होता है तो स्थानान्तरित होने वाली ऊर्जा को ऊष्मा (Heat) कहते हैं। दो निकायों के मध्य ऊष्मा का प्रवाह उच्च ताप से निम्न ताप की ओर होता है।
कार्य (Work)— यह भी दो निकायों के मध्य स्थानान्तरित होने वाली ऊर्जा है। जब किन्हीं दो निकायों के बीच ऊर्जा का स्थानान्तरण उनके तापान्तर पर निर्भर नहीं करता है तो उनके बीच स्थानान्तरित होने वाली ऊर्जा को कार्य कहते हैं।
आन्तरिक ऊर्जा (Internal Energy)— जब किसी तंत्र (निकाय) को ऊष्मा दी जाती है तो उसके कुछ भाग का उपयोग निकाय द्वारा परिवेश के विरुद्ध कार्य करने में होता है बाकी ऊष्मा से निकाय की आन्तरिक ऊर्जा में वृद्धि होती है। निकाय के अणुओं से सम्बद्ध ऊर्जा को आन्तरिक ऊर्जा कहा गया है। आन्तरिक ऊर्जा निकाय के अणुओं की स्थितिज तथा गतिज ऊर्जाओं के योग के बराबर होती है।
प्रश्न 5.
ऊष्मागतिकीय निकाय, ऊष्मागतिकीय चर राशियाँ व ऊष्मागतिकीय प्रक्रम से आप क्या समझते हैं?
उत्तर:
ऊष्मागतिकीय निकाय (Thermodynamical system)- सामान्यतया हम किसी वस्तु अथवा वस्तुओं के समूह को अन्य भागों से पृथक् कर उनमें परिवर्तन का अध्ययन करते हैं । इस वस्तु अथवा वस्तुओं के समूह को निकाय कहा जाता है एवं निकाय को जिस भाग से पृथक् किया गया है, उस भाग को परिवेश (surroundings) कहते हैं।
ऊष्मागतिकीय चर राशियाँ (Thermodynamical state variables)- हम जानते हैं कि ऊष्मागतिकीय निकाय, स्थूल निकाय होते हैं। इनका अध्ययन स्थूल गुणों दाब (P), आयतन (V), ताप (T) आदि के आधार पर किया जाता हैं। दाब, आयतन तथा ताप को अवस्था चर के नाम से जाना जाता है। अर्थात् किसी भी निकाय की अवस्था को (P, V, T) चरों द्वारा प्रदर्शित किया जाता है।
ऊष्मागतिकीय प्रक्रम (Thermodynamical process)- जब किसी ऊष्मागतिकीय निकाय के ऊष्मागतिकीय चरों में परिवर्तन कर उस निकाय में परिवर्तन किया जाता है तो इसे ऊष्मागतिकीय प्रक्रम, कहा जाता है। कुछ महत्त्वपूर्ण ऊष्मागतिकीय प्रक्रमों के नाम अग्रानुसार
- समातापीय प्रक्रम (Isothermal process)
- रुद्धोष्म प्रक्रम (Adiabatic process)
- समआयतनिक प्रक्रम (Isochoric process)
- समदाबीय प्रक्रम (Isobaric process)
- चक्रीय प्रक्रम (Cyclic process)
प्रश्न 6.
समतापीय प्रक्रम में किये गये कार्य को समझाइये।
उत्तर:
यदि नियत ताप पर किसी गैस के दाब व आयतन में परिवर्तन किया जाये तो यह समतापीय प्रक्रम कहलाता है। इसका अवस्था समीकरण PV = नियतांक होता है।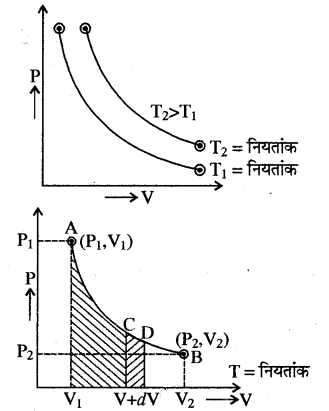
समतापीय प्रक्रमों को उपरोक्त ग्राफों से समझा जा सकता है। गैस को बिन्दु C से D तक की अवस्था में परिवर्तन हेतु किया गया। कार्य–
dW = PdV
तथा A से B तक परिवर्तन हेतु किया गया कार्य
w = (int _{ 0 }^{ W } d{ W }=int _{ V_{ 1 } }^{ V_{ 2 } } PdV=n{ RT }ln { left( frac { V_{ 2 } }{ V_{ 1 } } right) } )
समतापीय प्रक्रम में आन्तरिक ऊर्जा में कोई परिवर्तन नहीं होता। है। अतः ऊष्मागतिकी के प्रथम नियम से गैस को दी गई ऊष्मा गैस द्वारा किये गये कार्य के समान होती है।
प्रश्न 7.
ऊष्मागतिकी के प्रथम नियम की व्याख्या कीजिये।
उत्तर:
ऊष्मागतिकी का प्रथम नियम (First Law of thermodynamics)- ऊष्मागतिकी का प्रथम नियम ऊर्जा संरक्षण का नियम है। इसके अनुसार न तो ऊर्जा उत्पन्न की जा सकती है और न ही नष्ट की जा सकती है। जब किसी तंत्र को ΔQ ऊष्मा दी जाती है तो उसका कुछ भाग वायुमण्डलीय दाब के विपरीत कार्य ΔW करता है। जिसके कारण आयतन में वृद्धि होती है और शेष भाग गैस के ताप में वृद्धि करता है। ताप में वृद्धि होने के कारण आन्तरिक ऊर्जा में वृद्धि (dμ) होती है। अतः ऊर्जा के संरक्षण के नियमानुसार
ΔQ= dU + ΔW
अतः तंत्र को दी गई ऊष्मा (ΔQ), उसके आन्तरिक ऊर्जा में परिवर्तन (dU) तथा उस पर किये गये कार्य (ΔW) के योग के बराबर होता है।”
प्रश्न 8.
मेयर के सम्बन्ध की व्युत्पत्ति कीजिये।
उत्तर:
ऊष्मागतिकी के प्रथम नियम से
ΔQ= dU + ΔW ………. (1)
यदि एक निकाय में किसी आदर्श गैस के ॥ मोल, P दाब, V आयतन तथा T ताप पर लेकर विचार करें तो समआयतनिक परिवर्तनों के लिए,
dU = μCvΔT
समदाबीय परिवर्तनों के लिए, ΔQ = μCpΔT
एवं कार्य को सूत्र, ΔW = μRΔT
ये सभी मान समीकरण (1) में स्थापित करने पर
μCpΔT = μCvΔT + μRΔT
या Cp – Cv = R
इसी समीकरण को मेयर का सम्बन्ध कहा जाता है। इसके अनुसार किसी गैस की दोनों मोलर विशिष्ट ऊष्माओं (Cp तथा Cv) को अन्तर गैस नियतांक (R) के समान होता है।
प्रश्न 9.
उत्क्रमणीय व अनुक्रमणीय इंजन में अन्तर स्पष्ट कीजिये?
उत्तर:
लघूत्तरात्मक प्रश्न संख्या 1 का अध्ययन करें।
उत्क्रमणीय प्रक्रम- वह प्रक्रम जिसमें सभी प्रक्रियायें उत्क्रमणीय हों।
अनुक्रमणीय प्रक्रम- वह प्रक्रम जिसमें कम से कम एक प्रक्रिया अनुक्रमणीय हो।
उत्क्रमणीय इंजन- वह इंजन जो उत्क्रमणीय प्रक्रम के अनुसार कार्य करे।
अनुक्रमणीय इंजन- वह इंजन जो अनुत्क्रमणीय प्रक्रम के अनुसार कार्य करे।
प्रश्न 10.
किसी गैस के रुद्घोष्ण प्रसार को समझाते हुये किये गये कार्य की व्याख्या कीजिये।
उत्तर:
यदि किसी प्रक्रम में निकाय एवं परिवेश में ऊष्मा का आदान-प्रदान नहीं होता है (ΔQ = 0), तो इसे रुद्धोष्म प्रक्रम कहते हैं। इसके लिए आवश्यक प्रतिबन्ध निम्न हैं
(1) गैस का पात्र पूर्ण कुचालक होना चाहिए जिससे गैस तथा परिवेश में ऊष्मा का आदान-प्रदान न हो सके।
(2) प्रक्रम अतिशीघ्र होना चाहिए जिससे गैस को परिवेश के साथ ऊष्मा के आदान-प्रदान करने का समय ही न मिल सके।
रुद्धोष्म प्रक्रमों का अवस्था समीकरण PVγ है, एवं प्रक्रम का P, Vवक्र निम्नानुसार है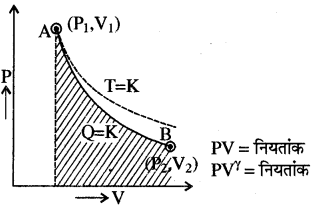
इस प्रक्रम में A से B बिन्दु तक अवस्था परिवर्तन के लिए किया गया कार्य
W = (int_{V_{1}}^{V_{r}} P d V=frac{P_{1} V_{1}-P_{2} V_{2}}{r-1}=frac{mu Rleft(T_{1}-T_{2}right)}{r-1})
प्रश्न 11.
कार्यों इंजन की दक्षता का सूत्र व्युत्पन्न करते हुए व्याख्या कीजिये।
उत्तर:
किसी इंजन की अधिकतम दक्षता प्राप्त करने हेतु सॉडी कार्गो (Sody Carnot) वैज्ञानिक ने एक आदर्श इंजन की परिकल्पना की। उसने इस संकल्पना को व्यावहारिक रूप देने के लिए आदर्श गैस को कार्यकारी पदार्थ के रूप में प्रयुक्त कर एक उत्क्रमणीय निकाय को आदर्श इंजन मान लिया। इंजन की दक्षता का मान स्रोत तथा सिंक के ताप (क्रमशः T1 तथा T2) पर निर्भर करता है। यह एक आदर्श इंजन है तथा हकीकत में ऐसा इंजन बनाना सम्भव नहीं है।
कार्नो इंजन की दक्षता (η) का सूत्र
कानें इंजन की दक्षता केवल स्रोत तथा सिंक के ताप पर निर्भर करती है। यह कार्यकारी पदार्थ की प्रकृति पर निर्भर नहीं करती है।
RBSE Class 11 Physics Chapter 13 निबन्धात्मक प्रश्न
प्रश्न 1.
ऊष्मागतिकी के शून्यांकी, प्रथम व द्वितीय नियम की विस्तारपूर्वक व्याख्या कीजिये।
उत्तर:
शून्यांकी नियम ऊष्मागतिकी का मूलभूत सिद्धान्त है एवं ताप को परिभाषित करता है। इसके अनुसार यदि दो निकाय A व B अलगअलग तीसरे निकाय C के साथ, तापीय सन्तुलन में हैं तो A व B भी आपस में तापीय संतुलन में होंगे।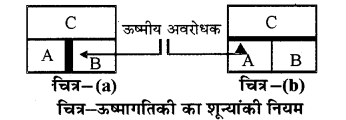
चित्र में दो निकाय A तथा B तीसरे निकाय C से सम्पर्क में हैं। एवं A तथा B के मध्य एक ऊष्मीय अवरोधक रखा हुआ है जिसके कारण A व B में ऊष्मी का आदान-प्रदान नहीं होता है। माना C का ताप और B से अधिक है, इस अवस्था में c से A एवं C से B की ओर ऊष्मा का प्रवाह तब तक होता है जब तक कि C व A तथा C व B आपस में ऊष्मीय संन्तुलन में न आएँ।
अब A व B के मध्य रखे हुए ऊष्मीय अवरोधक को हटाकर C तथा A, B के मध्य रख देते हैं, जैसा कि चित्र b में है। अब A व B के मध्य ऊष्मा का आदान-प्रदान नहीं होता है। अतः निकाय A व B ऊष्मीय सन्तुलन की अवस्था में आ गये हैं। यह प्रयोग ऊष्मागतिकी के शून्यांकी नियम को प्रदर्शित करता है।
”ऊष्मागतिकी के शून्यांकी नियम से यदि दो निकाय किसी अन्य तीसरे निकाय से अलग-अलग ऊष्मीय सन्तुलन में हों तो वे आपस में | भी ऊष्मीय सन्तुलन में होंगे।”
यह ताप के गुण को बताता है। यदि A से B की ओर ऊष्मा प्रवाहित होती है तो A का ताप B से अधिक है। यदि ऊष्मा प्रवाह नहीं होता है तो A और B का ताप एकसमान है।
ताप एक अदिश राशि है। ऊष्मागतिकी के शून्यांकी नियम से यदि दो निकाय आपस में ऊष्मीय सन्तुलन में हों तो उनके ताप भी समान होंगे, ताप वह गुण है जो ऊष्मा के एक निकाय से दूसरे निकाय के प्रवाह को निर्धारित करता है।
यदि A से B की ओर ऊष्मा प्रवाहित होती है तो A का ताप B से अधिक होता है। यदि ऊष्मा का प्रवाह नहीं हो तो A व B का ताप समान है। यदि A से B की ओर ऊष्मा प्रवाहित होती है तो यह आवश्यक नहीं है कि A की ऊष्मा अधिक है या B की।
ऊष्मागतिकी का प्रथम नियम ऊर्जा संरक्षण का नियम है। इसके अनुसार न तो ऊर्जा उत्पन्न की जा सकती है और न ही नष्ट की जा सकती है, सिर्फ ऊर्जा एक रूप से दूसरे रूप में बदली जा सकती है। जब किसी तंत्र को ΔQ ऊष्मा दी जाती है तो उसका कुछ भाग वायुमण्डलीय दाब के विपरीत कार्य ΔW करता है जिसके कारण आयतन में वृद्धि होती है और शेष भाग गैस के ताप में वृद्धि करता है। ताप में वृद्धि होने के कारण आन्तरिक ऊर्जा में भी वृद्धि होती है। ऊर्जा संरक्षण से,
ΔQ = dU + ΔW ………. (1)
इसको ऊष्मागतिकी का प्रथम नियम कहते हैं।
अतः ”तंत्र को दी गई ऊष्मा का योग, उसके आन्तरिक ऊर्जा में परिवर्तन व उस पर किये गये कार्य के योग के बराबर होता है। यदि ऊष्मा और आन्तरिक ऊर्जा को कैलोरी में और कार्य को जूल में लें,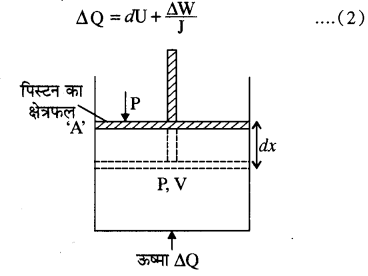
चित्रानुसार एक बेलनाकार पात्र में एक पिस्टन लगा रखा है। पिस्टन का क्षेत्रफल A है, गैस का दाब P है। पिस्टन के dx दूरी से विस्थापित करने पर।
dW = F dx
= (PA) dx
= PdV [∵ dV = Adx]
अर्थात्, ΔQ= du + (frac{mathrm{P} d mathrm{V}}{mathrm{J}})
दी गई ऊष्मा ΔQ और किया गया कार्य ΔW तंत्र को एक अवस्था से दूसरी अवस्था तक ले जाने वाले पथ पर निर्भर करते हैं। आंतरिक ऊर्जा तंत्र की प्रारंभिक एवं अंतिम अवस्था पर ही निर्भर करती है। कार्य व ऊष्मा को क्रमशः ΔW व ΔQ से तथा आन्तरिक ऊर्जा में परिवर्तन को dU से प्रदर्शित करते हैं ।
समीकरण (2) से स्पष्ट है कि
(i) यदि निकाय द्वारा कार्य किया जाता है तो कार्य को धनात्मक लिया जाता है। यदि निकाय पर कार्य किया जाता है तो यह ऋणात्मक होता है।
(ii) यदि निकाय के द्वारा ऊष्मा ली गई है तो ΔQ धनात्मक, यदि निकाय के द्वारा ऊष्मा दी गई है तो ΔQ ऋणात्मक होगी।
(iii) यदि निकाय की आन्तरिक ऊर्जा में वृद्धि होती है, तो dU धनात्मक तथा यदि आन्तरिक ऊर्जा में कमी आती है तो dU ऋणात्मक होती है।
(iv) द्रवों तथा ठोसों के आयतन में परिवर्तन नगण्य होता है। जिसके कारण ΔW का मान भी नगण्य होता है, अतः द्रवों व ठोसों के लिए ΔQ = dU होगा।
अर्थात् ऊष्मा में परिवर्तन आन्तरिक ऊर्जा में परिवर्तन के बराबर होगा।
ऊष्मागतिकी के प्रथम नियम से हम कह सकते हैं कि ”ऊष्मा, ऊर्जा का ही एक रूप है।” ”ऊष्मागतिकी निकाय में आन्तरिक ऊर्जा होती है जो कि निकाय की अवस्था पर ही निर्भर करती है तथा ऊष्मागतिकी निकाय में कुल ऊर्जा संरक्षित रहती है।”
ऊष्मागतिकी के द्वितीय नियम के बहुत से कथन हैं जो शाब्दिक रूप से भिन्न-भिन्न प्रतीत होते हैं। लेकिन भावार्थ की दृष्टि से एक ही हैं। सभी कथनों का मूलभाव इस प्रकार है
कोई भी ऐसा ऊष्मा-इंजन बनाना असम्भव है जो किसी स्रोत | से अवशोषित ऊष्मा को पूरी तरह लाभकारी कार्य में बदल दे। दूसरे शब्दों में, 100% दक्षता वाला ऊष्मा-इंजन बनाना असम्भव है।”
इस नियम के विभिन्न कथन निम्नवत् हैं|
(1) केल्विन एवं प्लांक का कथन- चक्रीय प्रक्रम में कार्य करने वाला ऐसा.इंजन बनाना असम्भव है, जिसके चलने से ऊष्मा स्रोत से ऊष्मा का शोषण और उस ऊष्मा से कार्य की प्राप्ति के अतिरिक्त कोई अन्य क्रिया नहीं हो। इंजन के लिये यह आवश्यक है कि कार्य की प्राप्ति के लिये, स्रोत से ऊष्मा का अवशोषण करे एवं उसके कुछ अंश को कार्य में परिणित कर शेष भाग को सिंक में त्याग दे। अर्थात् इंजन के लिये स्रोत एवं सिंक दोनों का होना आवश्यक है।
(2) क्लासियस का कथन- किसी चक्रीय प्रक्रम में बिना बाह्य कार्य किये कार्यकारी पदार्थ निम्न ताप वाली वस्तु से सीधे ही उच्च ताप वाली वस्तु को ऊष्मा स्थानान्तरित नहीं कर सकता।”
उदाहरण के लिये प्रशीतक (refrigerator) ठंडी वस्तु में से । ऊष्मा अवशोषित कर गर्म वस्तु (कमरा) को प्रदान करता है। लेकिन इसके लिये प्रशीतक, संपीडक (Compressor) का सहयोग लेता है। बाह्य सहायता (संपीडक के रूप में) के बिना प्रशीतक वस्तुओं को और ठंडी नहीं कर सकता है।
द्वितीय नियम के दोनों कथन एक-दूसरे के तुल्य हैं। ऊष्मागतिकी का द्वितीय नियम ऊष्मागतिकी के प्रथम नियम की अपूर्णता को दूर करता है। वास्तव में प्रथम नियम यह बताता है कि कार्य की प्राप्ति के लिये एक तुल्य ऊष्मा व्यय होती है। परन्तु यह इस रूपान्तरण की सीमाओं के विषय में कुछ नहीं बताता। ऊष्मागतिकी का द्वितीय नियम रूपान्तरण की सीमाओं को व्यक्त करता है और यह भी दर्शाता है कि कब और कितना रूपान्तरण सम्भव है। इस प्रकार दोनों एकदूसरे के पूरक हैं और दोनों मिलकर पूर्ण रूप से कार्य और ऊष्मा के रूपान्तरण को दर्शाते हैं।
प्रश्न 2.
ऊष्मागतिकी के विभिन्न प्रक्रमों व उनमें किये गये कार्य की व्याख्या कीजिये।
उत्तर:
विभिन्न ऊष
जब किसी ऊष्मागतिकीय निकाय के ऊष्मागतिकीय चरों में परिवर्तन के कारण उस निकाय की अवस्था में परिवर्तन होता है तो इसे । ऊष्मागतिकीय प्रक्रम कहते हैं। नीचे कुछ महत्त्वपूर्ण ऊष्मागतिकीय प्रक्रम दिये जा रहे हैं—
- समतापीय प्रक्रम (Isothermal Process)
- रुद्धोष्म प्रक्रम (Adiabatic Process)
- सम आयतनिक प्रक्रम (Isochoric Process)
- समदाबी प्रक्रम (Isobaric Process)
- चक्रीय प्रक्रम (Cyclic Process)
प्रश्न 3.
समतापी व रुद्धोष्म प्रक्रम में अन्तर स्पष्ट करते हुये उक्त प्रक्रमों में किये गये कार्य की गणना कीजिये।
उत्तर:
समतापीय प्रक्रम (Isothermal Process)
नियत ताप पर किसी गैस के दाब एवं आयतन में परिवर्तन किया। जाये तो यह समतापी प्रक्रम कहलाता है। इस प्रक्रम के लिये निम्न आवश्यक प्रतिबंध होते हैं
- प्रक्रम धीमी गति से किया जाना चाहिए जिससे कि निकाय को आवश्यकता अनुसार, परिवेश से ऊष्मा के आदान-प्रदान के लिये समय उपलब्ध हो सके।
- पात्र की दीवारें पूर्ण रूप से सुचालक होनी चाहिए जिससे कि परिवेश के साथ, प्रभावी ऊष्मीय सम्पर्क में रह सके।
उदाहरण
(i) किसी गैस का धीमी गति से किया गया संपीडन अथवा प्रसार-जब किसी गैस को दाब लगाकर संपीडित किया जाता है, तब उत्पन्न ऊष्मा परिवेश में त्याग दी जाये तो गैस का ताप नियत रहता है। इसी प्रकार यदि गैस का प्रसार होता है, तब परिवेश के विरुद्ध कार्य करना पड़ता है जिससे गैस के ताप में कमी होती है। यदि गैस परिवेश से ऊष्मी अवशोषित कर ले तो गैस का तापनियत रहता है।
(ii) अवस्था परिवर्तन (ठोस से द्रव या द्रव से गैस आदि) के समय पर भी निकाय का ताप स्थिर रहता है, अतः यह भी समतापी प्रक्रम ही होते हैं। जैसे-बर्फ का गलना, मोम का जमना, जल का वाष्प में बदलना।
समतापीय प्रक्रम के लिए अवस्था समीकरण (Equation of State for Isothermal Process)
चूँकि समतापीय परिवर्तन में गैस का ताप नियत रहता है, अतः आदर्श गैस में समतापीय परिवर्तन बॉयल के नियम के अनुसार होता है। अर्थात् गैस के निश्चित द्रव्यमान के लिये
PV = नियतांक
अतः यही समीकरण समतापीय प्रक्रम की अवस्था समीकरण होती है। अतः इस प्रक्रम के लिये P1V1 = P2V2 = P3V3
समतापीय प्रक्रम में गैस का दाब P तथा आयतन V में खींचा गया ग्राफ एक अतिपरवलय प्राप्त होता है। इस वक्र को समतापीय वक्र कहते हैं। चूँकि समतापीय परिवर्तन बहुत धीरे-धीरे होता है, अतः समतापीय वक्र का ढाल बहुत कम होता है। इसलिये समतापीय वक्र कम ढाल का होता है। एक ही ग्राफ पेपर पर खींचे गये दो समतापीय वक्र एक-दूसरे पत्र को कभी नहीं काटते हैं। इसका कारण यह है कि यदि दो समतापी वक्र काटेंगे तो कटाव बिन्दु पर P व V के एक ही मान के संगत दो ताप होंगे जो कि समीकरण PV = RT के अनुसार सम्भव नहीं है।
समतापीय वक़ को ढाल
m = tanθ = (frac{d P}{d V}) …………..(1)
समतापीय प्रक्रम का अवस्था समीकरण
PV = नियतांक (k)
अवकलन करने पर
PdV + VdP = 0
⇒ Vdp = -PdV
⇒ (frac{d P}{d V}=frac{-P}{V})
समी. (1) से m = tan θ = (frac{d P}{d V}=frac{-P}{V})
अर्थात् समतापीय वक्र की प्रवणता, दाब (P) वे आयतन (V) के । अनुपात के बराबर होती है तथा ऋणात्मक होती है।
विशिष्ट ऊष्मा C = (frac{Delta Q}{m d T}) = ∞
∵ समतापीय प्रक्रम के लिये T= नियतांक तब dT = 0
समतापीय प्रक्रम में किया गया कार्य (Work done in an Isothermal Process)
हम एक आदर्श गैस पर विचार करते हैं, जिसकी x ग्राम मोल मात्रा एक सुचालक पात्र में भरी हुई है। इस पात्र में एक सुचालक घर्षण मुक्त पिस्टन ऊपर-नीचे गति कर सकता है। भीतरी दाब, वायुमण्डलीय दाब से अधिक होने के कारण, गैस का प्रसार होता है एवं पिस्टन अपनी प्रारम्भिक अवस्था A से अंतिम अवस्था B तक विस्थापित हो जाता है।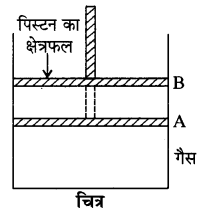
माना गैस का प्रारम्भिक व अन्तिम आयतन क्रमशः V1 तथा V2 एवं दाब P1 तथा P2 है।
माना पिस्टन का अनुप्रस्थ काट का क्षेत्रफल A है तथा प्रसारण के अन्तर्गत किसी समय दाब P है। अतः पिस्टन पर कार्य करने वाला बल
F = P × A ……………(1)
अतः पिस्टन के dx विस्थापन के लिये कार्य
dW = PAdx
या dW = PdV …………..(2)
[जहाँ Adx = dV= आयतन में परिवर्तन]
लेकिन आदर्श गैस के लिये

आदर्श गैस के समतापी प्रक्रम में आंतरिक ऊर्जा में कोई परिवर्तन नहीं होता है।
अतः ऊष्मागतिकी के प्रथम नियम से गैस को दी गई ऊष्मा की मात्रा गैस द्वारा किये गये कार्य के बराबर होती है। अतः
Q = W = 2303 nRTlog10(left(frac{V_{2}}{V_{1}}right))
जब V2 > V1अर्थात् आयतन बढ़ाने पर] तो W > 0 इस स्थिति में ऊष्मा का अवशोषण होगा।
जब V2 < V1 [अर्थात् आयतन कम करने पर] तो W < 0 इस स्थिति में ऊष्मा का निष्कासन होगा।
रुद्धोष्म प्रक्रम (Adiabatic Process) यदि किसी प्रक्रम में निकाय, परिवेश से ऊष्मा का आदान- प्रदान नहीं करता है तो इसे रुद्धोष्म प्रक्रम कहते हैं। इसके लिए आवश्यक प्रतिबन्ध निम्न हैं
(i) पात्र जिसमें निकाय (गैस) स्थित है पूर्ण कुचालक पदार्थ से निर्मित होना चाहिये जिससे कि गैस परिवेश से ऊष्मा का आदान-प्रदान नहीं कर सके।
(ii) ये प्रक्रम अचानक अर्थात् अति तीव्र गति से होने चाहिये जिससे कि गैस को परिवेश से ऊर्जा आदान-प्रदान के लिये समय ही न मिल सके रुद्धोष्म प्रक्रम
(Adiabatic Process)— रुद्धष्म प्रक्रम वे प्रक्रम होते हैं जिनमें निकाय, परिवेश के साथ ऊर्जा का आदान-प्रदान नहीं कर सकता है, अतः इनके लिये ΔQ = 0 इसलिये ऊष्मागतिक के प्रथम नियम से ΔQ = dU + ΔW 0 = dU + ΔW या dU = -ΔW = – PdV अर्थात् रुद्धोष्म प्रक्रम में निकाय द्वारा किया गया कार्य उसकी आन्तरिक ऊर्जा में कमी कर देता है जिससे निकाय का ताप कम हो जाता है। इसी प्रकार रुद्धोष्म संपीडन में निकाय पर कार्य किया जाता है। अर्थात् ΔW ऋणात्मक होगा। -ΔW = dU अर्थात् रुद्घोष्म संपीडन में निकाय पर किया गया कार्य उसकी आन्तरिक ऊर्जा में वृद्धि के बराबर होता है, अतः निकाय का ताप बढ़ जाता है।
उदाहरण
(i) ध्वनि तरंगों का किसी माध्यम से संचारित होना।
(ii) साइकिल के ट्यूब को अचानक फट जाना।
रुद्धोष्म प्रक्रम में किया गया कार्य (Work done in Adiabatic Process) हम जानते हैं कि ऊष्मागतिक प्रक्रमों के लिये

यह ताप के पदों में रुद्धोष्म प्रक्रम में किये गये कार्य के लिए व्यंजक है। चूंकि (frac{mathrm{R}}{gamma-1}) एक स्थिरांक है, अतः किया गया कार्य केवल प्रारम्भिक प्रथा अन्तिम तापों पर निर्भर करता है। यदि रुद्धोष्म प्रक्रम में कार्य गैस द्वारा सम्पन्न होता है (W > 0) तब T1 > T2 अर्थात् गैस का ताप घटता है। यदि कार्य गैस पर किया जाता है (W < 0) तब T1 < T2 अर्थात् गैस का ताप बढ़ जाता है।
प्रश्न 4.
कार्यों के उत्क्रमणीय इंजन की कार्यविधि लिखते हुये प्रत्येक प्रक्रम में किये गये कार्य को P-V वक़ द्वारा ज्ञात कीजिये तथा दक्षता का सूत्र व्युत्पन्न कीजिये।
उत्तर:
कार्नो चक्र (Carnot’s Cycle)
इस चक्र की सहायता से कार्यों इंजन की कार्यविधि को समझा जा सकता है। माना सिलिण्डर में एक ग्राम मोल आदर्श गैस भरी है। इसके प्रारम्भिक ऊष्मागतिक (P1, V1, T1) है। चित्र में इसकी अवस्था को A से दिखाया गया है। इस चक्र में कार्यकारी पदार्थ पर चार प्रक्रम किये जाते हैं। इनमें से दो प्रक्रम समतापी तथा दो प्रक्रम रुद्धोष्म होते हैं। इन प्रक्रमों का क्रम निम्न प्रकार होता है
- समतापी प्रसार
- रुद्धोष्म प्रसार
- समतापी संपीडन
- रुद्धोष्म संपीडन
(1) समतापी प्रसार ( अवस्था A से 8 तक)- प्रथम चरण में कार्यकारी पदार्थ को स्रोत पर रखा जाता है जिससे उसका ताप स्रोत का ताप T1K हो जाता है। इस स्थिति में गैस का समतापी प्रसार होता है। इस स्थिति में Q1 = W1
∵ समतापी प्रसार में dU = 0
चित्र में इसे AB द्वारा दर्शाया गया है।
माना कि इस प्रक्रिया के अन्त में बिन्दु B पर कार्यकारी पदार्थ को दाब P2 व आयतन V2 हो जाता है। अतः उपरोक्त प्रसार में गैस द्वारा किया गया कार्य स्रोत से अवशोषित ऊष्मा Q1 के बराबर होगा। कार्य गैस द्वारा किया जा रहा है। अतः यह धनात्मक होगा। चित्र में उक्त समतापी वक्र को AB द्वारा प्रदर्शित किया गया है।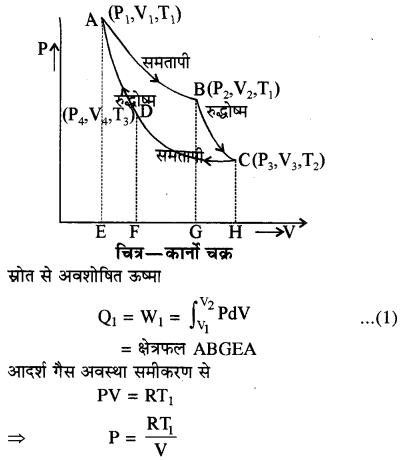
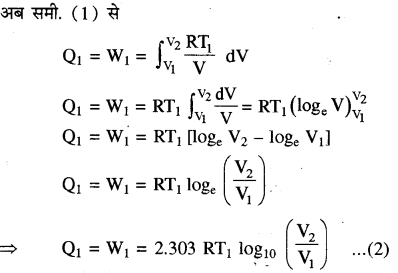
(2) रुद्धोष्म प्रसार (अवस्था B से C तक )- द्वितीय चरण में सिलिण्डर को स्रोत पर से हटाकर कुचालक स्टैण्ड पर रख दिया जाता है। इस स्थिति में गैस ऊष्मा का आदान-प्रदान नहीं कर सकती। यहाँ पर सिलिण्डर व स्टेण्ड दोनों कुचालक दीवारों से बने हैं और सिलिण्डर की तली वातावरण के सम्पर्क में नहीं है। अतः अब गैस का रुद्धोष्म प्रसार होता है। इसे वक्र BC से दर्शाया गया है। इस प्रसार के कारण गैस की आन्तरिक ऊर्जा में कमी होती है जिसके कारण इसका ताप भी घटकर T1 से T2 हो जाता है। इस प्रक्रम में भी कार्य W2 गैस द्वारा किया जा रहा है। अतः कार्य धनात्मक होगा।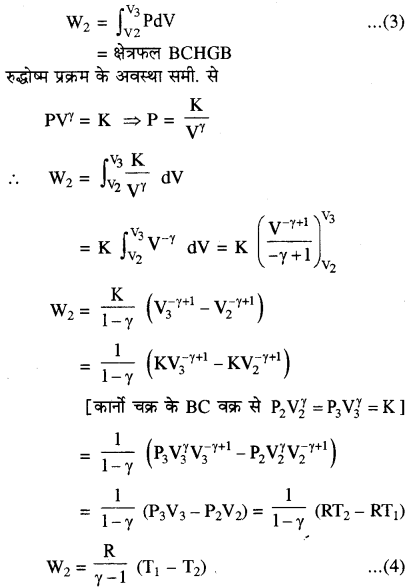
(3) समतापी संपीडन (अवस्था C से D तक)- द्वितीय चरण के पश्चात् गैस का दाब इतना कम हो जाता है कि अब यह और कार्य करने में असमर्थ हो जाती है और कोई कार्य की प्राप्ति के लिये गैस का प्रारम्भिक अवस्था में लौटना आवश्यक होता है। तीसरे चरण में सिलिण्डर को सिंक पर रखकर पिस्टन को धीरे-धीरे अन्दर की ओर धकेलते हैं। इस कारण गैस का संपीडन होने लगता है। संपीडन के कारण उत्पन्न ऊष्मा, गैस, सिंक में त्याग देती है। अतः यह संपीडन समतापी होता है, इसे वक्र में CD से प्रदर्शित किया गया है। सिंक को दी गयी ऊष्मा (Q2), गैस पर किये गये कार्य के तुल्य होती है एवं यह कार्य ऋणात्मक होता है।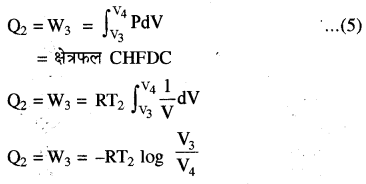
Q2 = W3 = -2.303 RT2 log10(left(frac{mathrm{V}_{3}}{mathrm{V}_{4}}right)) …………(6)
यहाँ पर ऋणात्मक चिन्ह यह व्यक्त करता है कि गैस पर कार्य किया गया है।
(4) रुद्धोष्म संपीडन (अवस्था D से A तक)- इस स्थिति में सिलिण्डर को पुनः कुचालक स्टेण्ड पर रखकर गैस का रुद्धोष्म संपीडन किया जाता है। इस संपीडन को तब तक किया जाता है जब तक कि गैस का ताप पुनः T1 नहीं हो जाता एवं गैस अपनी प्रारम्भिक अवस्था A को प्राप्त नहीं कर लेती है। इसे चित्र में DA से प्रदर्शित किया गया है।
इस प्रक्रिया में गैस का दाब व आयतन क्रमशः P1 व V1 हो | जाता है। इस प्रक्रम में किया गया कार्य W4 है तो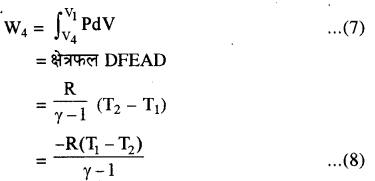
यहाँ ऋणात्मक चिन्ह यह व्यक्त करता है कि गैस पर कार् किया गया है।
अतः कार्नो चक्र में गैस द्वारा किया गया कुल कार्य
W = W1 + W2 + W3 + W4
मान रखने पर

समी. (9) को निम्न प्रकार से भी लिखा जा सकता है|
W = Q1 – Q2
कार्यों इंजन की दक्षता (n)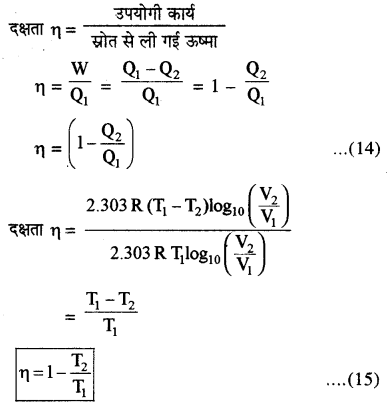
इस प्रकार समी. (14) दक्षता का मूल सूत्र है, जिससे सूत्र (15) प्राप्त किया गया है। इससे स्पष्ट होता है कि
(i) का इंजन की दक्षता केवल स्रोत तथा सिंक के ताप पर निर्भर करती है। यह कार्यकारी पदार्थ पर भी निर्भर नहीं करती है।
(ii) इंजन की दक्षता η का मान 1 तब ही होगा जबकि T2 = 0K, अर्थात् जब सिंक का ताप परम शून्य होगा जो कि असम्भव है। अतः दक्षता 100% असम्भव है।
(iii) T1 का मान T2 से अधिक होने के कारण दक्षता सदैव 1 से कम होती है।
विशेष-दक्षता के सूत्र (14) तथा (15) की तुलना से स्पष्ट है कि
(frac{Q_{2}}{Q_{1}}=frac{T_{2}}{T_{1}}) या (frac{Q_{1}}{T_{1}}=frac{Q_{2}}{T_{2}})
यह कार्नो चक्र का प्रतिबन्ध है|
प्रश्न 5.
ऊष्मागतिकी के द्वितीय नियम के केल्विन प्लांक व क्लासियस के कथनों को लिखिये तथा स्पष्ट कीजिये कि उक्त कथन एक दूसरे के तुल्य हैं।
उत्तर:
ऊष्मागतिकी के द्वितीय नियम के बहुत से कथन हैं जो शाब्दिक रूप से भिन्न-भिन्न प्रतीत होते हैं। लेकिन भावार्थ की दृष्टि से एक ही हैं। सभी कथनों का मूलभाव इस प्रकार है
“कोई भी ऐसी ऊष्मा-इंजन बनाना असम्भव है जो किसी स्रोत से अवशोषित ऊष्मा को पूरी तरह लाभकारी कार्य में बदल दे। दूसरे शब्दों में, 100% दक्षता वाला ऊष्मा-इंजन बनाना असम्भव है।”
इस नियम के विभिन्न कथन निम्नवत् हैं
(1) केल्विन एवं प्लांक का कथन- चक्रीय प्रक्रम में कार्य करने वाला ऐसा.इंजन बनाना असम्भव है, जिसके चलने से ऊष्मा स्रोत से ऊष्मा का शोषण और उस ऊष्मा से कार्य की प्राप्ति के अतिरिक्त कोई अन्य क्रिया नहीं हो। इंजन के लिये यह आवश्यक है कि कार्य की प्राप्ति के लिये, स्रोत से ऊष्मा का अवशोषण करे एवं उसके कुछ अंश को कार्य में परिणित कर शेष भाग को सिंक में त्याग दे। अर्थात् इंजन के | लिये स्रोत एवं सिंक दोनों का होना आवश्यक है।
(2) क्लासियस का कथन- “किसी चक्रीय प्रक्रम में बिना बाह्य कार्य किये कार्यकारी पदार्थ निम्न ताप वाली वस्तु से सीधे ही उच्च ताप वाली वस्तु को ऊष्मा स्थानान्तरित नहीं कर सकता।”
उदाहरण के लिये प्रशीतक (refrigerator) ठंडी वस्तु में से ऊष्मा अवशोषित कर गर्म वस्तु (कमरा) को प्रदान करता है। लेकिन इसके लिये प्रशीतक, संपीडक (Compressor) का सहयोग लेता है। बाह्य सहायता (संपीडक के रूप में) के बिना प्रशीतक वस्तुओं को और ठंडी नहीं कर सकता है।
द्वितीय नियम के दोनों कथन एक-दूसरे के तुल्य हैं। ऊष्मागतिकी का द्वितीय नियम ऊष्मागतिकी के प्रथम नियम की अपूर्णता को दूर करता है। वास्तव में प्रथम नियम यह बताता है कि कार्य की प्राप्ति के लिये एक तुल्य ऊष्मा व्यय होती है। परन्तु यह इस रूपान्तरण की सीमाओं के विषय में कुछ नहीं बताता। ऊष्मागतिकी का द्वितीय नियम रूपान्तरण की सीमाओं को व्यक्त करता है और यह भी दर्शाता है कि कब और कितना रूपान्तरण सम्भव है। इस प्रकार दोनों एकदूसरे के पूरक हैं और दोनों मिलकर पूर्ण रूप से कार्य और ऊष्मा के रूपान्तरण को दर्शाते हैं।
केल्विन तथा क्लासियस के कथनों की समतुल्यता ऊष्मागतिकी के द्वितीय नियम से केल्विन प्लांक एवं क्लासियस कथन एक-दूसरे के तुल्य हैं। इसे निम्न प्रकार से समझाया जा सकता हैं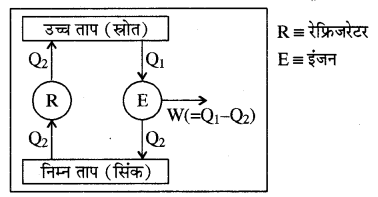
माना कि रेफ्रिजरेटर R निम्न ताप से Q2 ऊष्मा ग्रहण करके उच्च ताप को सारी ऊष्मा Q2(बिना बाह्य कार्य किये) स्थानान्तरित कर देता है। यह क्लासियस के कथन का उल्लंघन है। माना कि इंजन E जो इन्हीं दो तापों के मध्य कार्य करता है। यह इंजन उच्च ताप से Q1 ऊष्मा ग्रहण करके इसका कुछ भाग (Q1 – Q2) कार्य में परिवर्तित करके, शेष ऊष्मा Q2 को निम्न ताप पर स्थानान्तरित कर देता है।
अब इस इंजन के साथ आदर्श रेफ्रिजरेटर को युग्मित कर देते हैं। इसका परिणाम ज्ञात करने के लिए हम उपरोक्त चित्र से उच्च ताप से। कुल ऊष्मा प्राप्त करने की गणना करें जो कि Q1 – Q2 है। कुल कार्य में परिवर्तित ऊष्मा भी Q1 – Q2 है तथा निम्न ताप को लौटाई गई ऊष्मा Q2 – Q2 = शून्य| अर्थात् यह युक्ति उच्च ताप से Q1 – Q2) ऊष्मा ग्रहण कर निम्न ताप की वस्तु को बिना कोई ऊष्मा का अंश लौटाए सम्पूर्ण ऊष्मा Q1 – Q2 को कार्य में परिवर्तित कर देती है।
यह कथन केल्विन-प्लांक कथन का विरोधाभासी है।
इसी प्रकार माना कि एक इंजन E उच्च ताप से ऊष्मा Q1 ग्रहण करता है तथा बिना निम्न ताप को कोई ऊष्मा लौटाए सम्पूर्ण ऊष्मा (Q1) को कार्य में परिवर्तित कर देता है। यह कथन केल्विन-प्लांक कथन के विरोधाभासी है।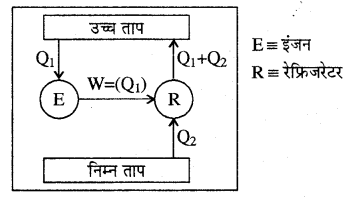
अब हम एक रेफ्रिजरेटर R की कल्पना कर रहे हैं जो कि पूर्व वाले उच्च तथा निम्न तापों के मध्ये काम कर रहा है। यह रेफ्रिजरेटर िम्न ताप की वस्तु से ऊष्मा Q2 ग्रहण करता है एवं इस पर Q1 बाह्य कार्य किया जाता है (अर्थात् W = Q1) और अंततः (Q1 + Q2) ऊष्मा उच्च ताप की वस्तु को लौटा देता है। अर्थात् यह रेफ्रिजरेटर किसी नियम का उल्लंघन नहीं करता है।
अब यदि इस इंजन तथा रेफ्रिजरेटर को युग्मित कर दिया जाये तो दोनों मिलकर निम्न ताप की वस्तु से Q2 ऊष्मा ग्रहण कर बिना किसी बाह्य ऊर्जा स्रोत के Q2[Q1 + Q2 – Q1] ऊष्मा उच्च ताप को स्थानान्तरित कर देता है। यह क्लासियस के कथन का स्पष्ट रूप से उल्लंघन है।
ऊष्मागतिकी को द्वितीय नियम ऊष्मागतिकी के प्रथम नियम का अनुपूरक है। प्रथम नियम यह दर्शाता है कि कोई भी युक्ति जितनी ऊर्जा प्राप्त करती है, उससे अधिक ऊर्जा नहीं त्याग सकती है। प्रथम नियम ऊर्जा त्यागने से सम्बन्धित कोई भी आवश्यक शर्त अथवा सीमा प्रयुक्त नहीं करता है। लेकिन द्वितीय नियम इस प्रकार की सीमा या शर्त प्रस्तुत करता है। उदाहरणार्थ-किसी भी पदार्थ द्वारा ग्रहण की गई सम्पूर्ण ऊष्मा को पूर्णतया कार्य में परिवर्तित करना असम्भव है। अर्थात् निम्न ताप से उच्च ताप की ओर ऊष्मा स्वतः प्रवाहित नहीं हो सकती। इस प्रकार की घटनाओं को प्रथम नियम अनुमति देता है, लेकिन द्वितीय नियम अनुमति नहीं देता है।
प्रश्न 6.
कार्गों प्रमेय का कथन लिखते हुये व्युत्पन्न कीजिये।
उत्तर:
कार्ने प्रमेय (Carnot’s Theorem)
इस प्रमेय की निम्न कथनों के अनुसार व्याख्या की जा सकती है. (अ) किन्हीं दो तापों T1 तथा T2 (T1 > T2) के मध्ये कार्य कर रहे इंजन की दक्षता, इन्हीं तापों के मध्य कार्य कर रहे कार्यो इंजन की दक्षता से अधिक नहीं हो सकती है। अर्थात् का इंजन (उत्क्रमणीय) की दक्षता अधिकतम होती है।
(ब) किन्हीं दो तापों T1 तथा T2 (T1 > T2) के मध्य कार्य करने वाले सभी कार्यों इंजनों (उत्क्रमणीय) की दक्षता समान होती है। यह दक्षता इंजन के कार्यकारी पदार्थ पर निर्भर नहीं करती है।
भाग (अ) की व्युत्पत्ति (Proof)
(अ) चित्रानुसार मानें कि दो इंजन जिनमें से एक अनुत्क्रमणीय (Irreversible) है, इसे I से प्रदर्शित किया गया है तथा दूसरा उत्क्रमणीय (Reversible) है, इसे R से प्रदर्शित किया गया है। दोनों T1 ताप के स्रोत तथा T2 ताप के सिंक के मध्य कार्य कर रहे हैं (T1 > T2)। दोनों में एक ही कार्यकारी पदार्थ है। दोनों इंजन प्रत्येक चक्र में समान कार्य (W) करते हैं।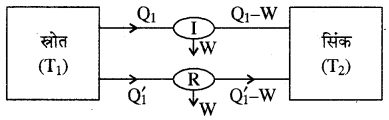
यदि अनुत्क्रमणीय (I) इंजन T1 ताप के स्रोत से Q1 ऊष्मा ग्रहण कर W कार्य करने के उपरान्त शेष (Q1 – W) ऊष्मा T2 ताप के सिंक को लौटा देता है तो अनुक्रमणीय इंजन की दक्षता (η1) होगी
η1 = (frac{mathrm{W}}{mathrm{Q}_{1}})
इसी प्रकार दूसरा उत्क्रमणीय (R) इंजन T; ताप के स्रोत से (mathrm{Q}_{1}^{prime}) ऊष्मा ग्रहण कर W कार्य करने के उपरान्त शेष (left(mathrm{Q}_{1}^{prime}-mathrm{W}right)) ऊष्मा T2 ताप के सिंक को स्थानान्तरित कर देता है तो उत्क्रमणीय इंजन की दक्षता (η2) होगी।
η2 = (frac{W}{Q_{1}^{prime}})
कल्पना करें कि η1 > η2
अर्थात् (frac{W}{Q_{1}}>frac{W}{Q_{1}^{prime}}) या (mathrm{Q}_{mathrm{i}}^{prime}>mathrm{Q}_{mathrm{l}})
अर्थात् (left(mathrm{Q}_{1}^{prime}-mathrm{Q}_{1}right)) एक धनात्मक राशि है।
अब इन दोनों इंजनों को निम्न व्यवस्थानुसार जोड़ दिया जाता है। I इंजन सीधी दिशा में तथा R इंजन विपरीत दिशा में कार्य करता है।
(उत्क्रमणीय इंजन को विपरीत दिशा में कार्य में लेकर प्रशीतक की भाँति काम में ले सकते हैं।)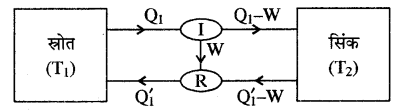
अर्थात् प्रथम इंजन (I) जो कार्य उत्पन्न करता है, उसी कार्य से विपरीत दिशा में कार्यरत इंजन (R) (जो कि प्रशीतक (Refrigerator) की भाँति कार्य कर रहा है संचालित हो रहा है। दोनों इंजन I तथा R एक स्वचालित मशीन की भाँति कार्यरत हैं।
इस स्वचालित मशीन में स्रोत द्वारा ली गई कुल ऊष्मा
= Q’1 – Q1
एवं सिंक द्वारा दी गई ऊष्मा = (Q’1 – W) – (Q1 – W)
= Q’1 – Q1
अर्थात् स्वचालित युक्ति निम्न ताप T2 वाले सिंक से Q’1 – Q1 प्राप्त कर उच्च ताप T1 वाले स्रोत को Q’1 – Q1 ऊष्मा प्रत्येक चक्र में स्थानान्तरित कर रही है एवं इस हेतु कोई बाह्य कार्य नहीं किया जा रहा है। यह ऊष्मागतिकी के द्वितीय नियम के सिद्धान्तों के विपरीत है।
इससे सिद्ध होता है कि दो नियत तापों T1 तथा T2 के मध्य कार्य करने वाले अनुक्रमणीय इंजन की दक्षता इन्हीं तोपों के मध्य कार्यरत उत्क्रमणीय इंजन की क्षमता से अधिक नहीं हो सकती है।
भाग (ब) की व्युत्पत्ति-कार्ने प्रमेय के भाग (ब) की व्युत्पत्ति करने हेतु हम दो उत्क्रमणीय इंजनों R तथा R’ की कल्पना करते हैं जो कि समान तापों T1 तथा T2 के मध्य युग्मित मशीन की। भाँति स्वचालित है एवं उनमें भिन्न-भिन्न कार्यकारी पदार्थ है।
माना कि ηR > ηR है, तो हम (जैसा कि प्रमेय के भाग (अ) में वर्णन किया गया है) इस निष्कर्ष पर पहुँचेंगे कि ऊर्जा को निम्न ताप से उच्च ताप तक बिना किसी बाह्य कार्य के स्थानान्तरित किया जा सकता है। अर्थात् ηR > ηR मानना त्रुटिपूर्ण है।
इसी प्रकार का निष्कर्ष हमें तब प्राप्त होगा जब हम मानेंगे कि ηR’ < ηR है।
अतः हम इस निष्कर्ष पर पहुँचते हैं कि दो नियत तापों के मध्य कार्यरत सभी उत्क्रमणीय इंजनों की दक्षता समान होती है चाहे उनमें भिन्न-भिन्न कार्यकारी पदार्थ हों।
RBSE Class 11 Physics Chapter 13 आंकिक प्रश्न
प्रश्न 1.
एक आदर्श इंजन की दक्षता 75% है तथा यह 283 K ताप पर सिंक को 2 × 103 w ऊष्मा निष्कासित करता है तो ।
(i) स्रोत का ताप, (ii) प्रति मिनट इंजन द्वारा किया गया कार्य तथा (iii) एक चक्र में स्रोत से अवशोषित ऊष्मा की गणना कीजिये।
हल:
η = 75% = (frac{3}{4})
T2 = 283 K
Q2 = 2 × 103 w
प्रश्न 2.
हिमांक व वाष्पांक के मध्य कार्य कर रहे कार्यों इंजन की दक्षता की गणना कीजिये।
हल:
दिया गया है
T1 = 373 K
T2 = 273 K
η = 1 – (frac{mathrm{T}_{2}}{mathrm{T}_{1}})
= 1 – (frac{273}{373}=frac{100}{373}) × 100
= 26.8% = 27%
प्रश्न 3.
एक कार्यों इंजन की दक्षता 40% है। यदि इसका स्रोत का ताप 193.6°C है तब सिंक का ताप ज्ञात करो।
हल:
दिया गया है
η = 40% = (frac{40}{100}=frac{2}{5})
T1 = 193.6 + 273 = 466.6
(frac{mathrm{T}_{2}}{mathrm{T}_{1}}) = 1 – η
T2 = (1 – η)
T1 = (1 – (frac{2}{5})) × 466.6
= (frac{3}{5}) × 466.6 = 279.96 K
279.96 – 273 = 7°C
प्रश्न 4.
एक कार्यों रेफ्रिजरेटर 260 K व 400 K तापों के मध्य कार्य करता है। यह निम्न ताप पर सिंक से 600 cal ऊष्मा लेता है तब उच्च ताप पर स्रोत की दी गई ऊष्मा व प्रत्येक चक्र में किये गये कार्य की गणना कीजिये।
हल:
दिया गया है
T2 = 260 K
T1 = 400 K
Q2 = 600 cal
सूत्र-
(frac{mathrm{Q}_{1}}{mathrm{Q}_{2}}=frac{mathrm{T}_{1}}{mathrm{T}_{2}})
Q1 = (frac{mathrm{T}_{1}}{mathrm{T}_{2}}) × Q2
= (frac{400}{260}) × 600 = 923.1 cal
W = Q1 – Q2
= 923.1 – 600 = 323.1 cal
= 323.1 × 4.2 J [∵ 1 cal = 4.2 J]
= 1357
प्रश्न 5.
किसी कार्यों इंजन की दक्षता 100 K व TK तथा 180 K व 900 K के लिये समान है तब T की गणना करिये।
हल:
दिया गया है
T2 = 100 K
T1 = T = ?
T’2 = 180
T’1 = 900 K
यदि η समान है तो
(frac{mathrm{T}_{2}}{mathrm{T}_{1}}=frac{mathrm{T}_{2}^{prime}}{mathrm{T}_{1}^{prime}})
(frac{100}{T}=frac{180}{900})
T = 100 × 5 = 500 K
प्रश्न 6.
दो का इंजन A व B श्रेणीक्रम में कार्यरत हैं। पहला इंजन A, 900 K पर ऊष्मा प्राप्त करता है व T K ताप पर स्थित कुंड को निरस्त कर देता है। दूसरा इंजन B पहले इंजन द्वारा निरस्त ऊष्मा को प्राप्त कर 400 K पर ऊष्मा कुंड को निरस्त कर देता है। निम्न स्थितियों में ताप T की गणना करो
(i) जब दोनों इंजनों द्वारा किया गया कार्य समान है।
(ii) दोनों इंजनों की दक्षता बराबर है।
हल:
इंजन A इंजन B
T1 = 900 K T’1 = T
T2 = T K T’2 = 400 K
(i) यदि कार्य समान हो तो
W = Q1 – Q2 ∝ T1 – T2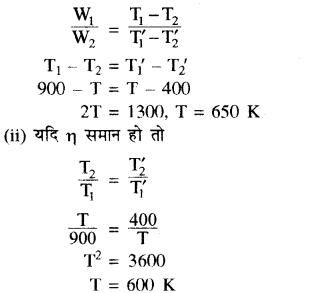
प्रश्न 7.
किसी गैस (γ = 1.5) को रुद्धोष्म प्रक्रम अनुसार संपीडित किया जाता है तो उसका आयतन 1600 cm3 से 400 cm3 हो जाता है। अब यदि प्रारम्भिक दाब को मान 150 KPa है तो अन्तिम दाब की गणना कीजिये तथा गैस पर किये गये कार्य की गणना कीजिये।
हल:
दिया गया है
γ = 1.5, V1 = 1600 cm3 = 1600 × 10-6 m3
V2 = 400 cm = 400 × 10-6 m3
P1 = 150 kPa
P2 = ?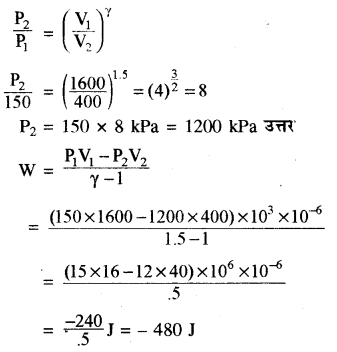
प्रश्न 8.
यदि किसी गैस (γ = 1.5) को उसके मूल दाब से 27 गुना दाब पर संपीडित किया जाता है तो उसके ताप में परिवर्तन की गणना कीजिये यदि प्रारम्भिक ताप 27°c है।
हल:
दिया गया है
γ = 1.5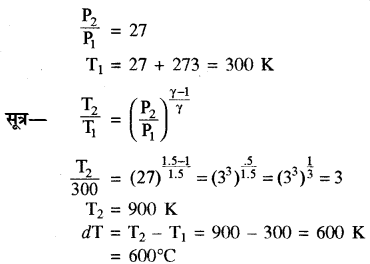
प्रश्न 9.
एक प्रशीतक ताप – 10°C से +27°C को प्रति सेकण्ड 200 J औसत ऊष्मा का स्थानान्तरण करता है। चक्र को उत्क्रमणीय मानते हुये औसत शक्ति की गणना कीजिये जबकि किसी अन्य प्रकार का ऊष्मा क्षय न हो रहा हो।
हल:
दिया गया है
T2 = – 10°C = – 10 + 273 = 263. K
T1 = 27°C = 27 + 273 = 300 K
Q2 = 200 J
सूत्र-
(frac{mathrm{Q}_{1}}{mathrm{Q}_{2}}=frac{mathrm{T}_{1}}{mathrm{T}_{2}})
Q1 = (frac{300}{263}) × 200
= 228.1 J/सेकण्ड
W = Q1 – Q2
= 228.1 – 200 = 28.1 J/सेकण्ड
= 28.1 W
प्रश्न 10.
किसी चक्रीय प्रक्रम का P-V वक़ निम्नानुसार है। तो चक्रीय प्रक्रम में किये गये कार्य की गणना करो।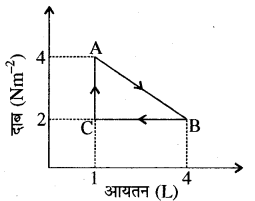
हल
W = कार्य = Δ का क्षेत्रफल ABC
= (frac{1}{2}) × CB × AC
= (frac{1}{2}) (3 × 103 × 2)
= 3 × 102 J
प्रश्न 11.
एक कार्यों इंजन 373 K व 283 K के मध्ये कार्य कर रहा है। उसकी दक्षता की गणना कीजिये और बताइये कि दक्षता कब 100% होगी?
हल:
दिया गया है
T1 = 373
T2 = 283
(अ) η = 1 – (frac{mathrm{T}_{2}}{mathrm{T}_{1}})
= 1 – (frac{283}{373}=frac{373-283}{373}=frac{90}{373})
= 24.12%
यदि दक्षता शून्य है तो (η = 0)
(ब) T2 = 0K
All Chapter RBSE Solutions For Class 12 Physics Hindi Medium
—————————————————————————–
All Subject RBSE Solutions For Class 11 Hindi Medium
*************************************************
————————————————————
All Chapter RBSE Solutions For Class 11 physics Hindi Medium
All Subject RBSE Solutions For Class 11 Hindi Medium
Remark:
हम उम्मीद रखते है कि यह RBSE Class 11 physics Solutions in Hindi आपकी स्टडी में उपयोगी साबित हुए होंगे | अगर आप लोगो को इससे रिलेटेड कोई भी किसी भी प्रकार का डॉउट हो तो कमेंट बॉक्स में कमेंट करके पूंछ सकते है |
यदि इन solutions से आपको हेल्प मिली हो तो आप इन्हे अपने Classmates & Friends के साथ शेयर कर सकते है और HindiLearning.in को सोशल मीडिया में शेयर कर सकते है, जिससे हमारा मोटिवेशन बढ़ेगा और हम आप लोगो के लिए ऐसे ही और मैटेरियल अपलोड कर पाएंगे |
आपके भविष्य के लिए शुभकामनाएं!!