हेलो स्टूडेंट्स, यहां हमने राजस्थान बोर्ड कक्षा 12वीं की रसायन विज्ञान सॉल्यूशंस को दिया हैं। यह solutions स्टूडेंट के परीक्षा में बहुत सहायक होंगे | Student RBSE solutions for Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी pdf Download करे| RBSE solutions for Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी notes will help you.
राजस्थान बोर्ड कक्षा 12 chemistry के सभी प्रश्न के उत्तर को विस्तार से समझाया गया है जिससे स्टूडेंट को आसानी से समझ आ जाये | सभी प्रश्न उत्तर Latest Rajasthan board Class 12 chemistry syllabus के आधार पर बताये गए है | यह सोलूशन्स को हिंदी मेडिअम के स्टूडेंट्स को ध्यान में रख कर बनाये है |
Table of Contents
Rajasthan Board RBSE Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी
RBSE Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी पाठ्यपुस्तक के अभ्यास प्रशन
RBSE Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी बहुविकल्पीय प्रश्न
प्रश्न 1.
शून्य कोटि अभिक्रिया के वेग स्थिरांक की इकाई होगी –
(a) mol L-1 s-1
(b) L mol-1 s-1
(c) s-1
(d) mol2 L-2 s-1
प्रश्न 2.
एक प्रथम कोटि अभिक्रिया की अर्द्ध आयु 69.3 s है, तो इसका वेग स्थिरांक है –
(a) 10-2 s-1
(b) 10-4 s-1
(c) 10 s-1
(d) 102 s-1
प्रश्न 3.
एक अभिक्रिया का वेग नियतांक 7.239 × 10-4 s-1 है, तो अभिक्रिया की कोटि होगी –
(a) 0
(b) 1
(c) 2
(d) 3
प्रश्न 4.
प्रथम कोटि अभिक्रिया के लिए कौन-सा कथन सत्य है?
(a) अभिक्रिया का वेग अभिकारकों की सान्द्रता की शून्य घात के अनुक्रमानुपाती है।
(b) वेग नियतांक की इकाई mol L-1 s-1 होती है।
(c) अभिक्रिया की अर्द्ध आयु अभिकारकों की आरम्भिक सान्द्रता पर निर्भर नहीं करती।
(d) सीधे तौर पर कुछ भी नहीं कहा जा सकता।
प्रश्न 5.
प्रथम कोटि अभिक्रिया के लिए Log k एवं 1/T में ग्राफ खींचते हैं, तो एक सरल रेखा प्राप्त होती है। प्राप्त रेखा की प्रवणता (ढाल) होगा-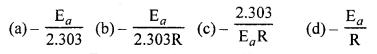
प्रश्न 6.
ताप में थोड़ी वृद्धि करने से अभिक्रिया का वेग तीव्रता से बढ़ता है, क्योंकि –
(a) सक्रियता अभिकारकों की संख्या में वृद्धि हो जाती है।
(b) संघट्टों की संख्या बढ़ जाती है।
(c) मुक्त पथ की लम्बाई बढ़ जाती है।
(d) अभिक्रिया ऊष्मा बढ़ जाती है।
प्रश्न 7.
शून्य कोटि अभिक्रिया के लिए निम्न में से कौन-सा सम्बन्ध सही है?
प्रश्न 8.
आर्मेनियस समीकरण है –
प्रश्न 9.
प्रथम कोटि अभिक्रिया की अर्द्ध आयु 480 s हो, तो वेग स्थिरांक होगा –
(a) 1.44 × 10-3 s-1
(b) 1.44 s-1
(c) 0.72 × 10-3 s-1
(d) 2.88 × 10-3 s-1
प्रश्न 10.
प्रथम कोटि अभिक्रिया के 90% पूर्ण होने में लगभग समय होगा –
(a) अर्द्ध आयु का 1.1 गुना
(b) अर्द्ध आयु का 3.3 गुना
(c) अर्द्ध आयु का 3.3 गुन्ना
(d) अर्द्ध आयु 4.4 गुना
उत्तर:
- (a)
- (a)
- (b)
- (c)
- (b)
- (a)
- (b)
- (b)
- (a)
- (c)
RBSE Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी अति लघुतरात्मक प्रश्न
प्रश्न 1.
एक अभिक्रिया A+ B → उत्पाद, के लिए वेग नियम r = k [A]1/2 [B]2 से दिया गया है। अभिक्रिया की कोटि क्या है?
उत्तर:
r = k [A]1/2 [B]2
अभिक्रिया की कोटि = [latex]frac { 1 }{ 2 } [/latex] + 2 = [latex]frac { 5 }{ 2 } [/latex]
प्रश्न 2.
अणु X का Y में रूपान्तरण द्वितीय कोटि की बलगतिकी के अनुरूप होता है। यदि x की सान्दता तीन गुनी कर दी जाये तो Y के निर्माण होने के वेग पर क्या प्रभाव पड़ेगा ?
उत्तर:

RBSE Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी लघूत्तरात्मक प्रश्न
प्रश्न 1.
R → P, अभिक्रिया के लिए अभिकारक की सान्दता 0:03 M से 25 मिनट में परिवर्तित होकर 0.02 M हो जाती है। औसत वेग की गणना सेकण्ड तथा मिनट दोनों इकाइयों में कीजिए।
उत्तर:

प्रश्न 2.
2A → उत्पाद, अभिक्रिया में A की सान्द्रता 10 min में 0.5 mol L-1 से घटकर 0.4 mol L-1 रह जाती है। इस समय अन्तराल के लिए अभिक्रिया वेग की गणना कीजिए।
उत्तर:
प्रश्न 3.
एक प्रथम कोटि की अभिक्रिया का वेग स्थिरांक 1.15 × 10-3 s-1 है। इस अभिक्रिया में अभिकारक की 5g मात्रा को घटकर 3g होने में कितना समय लगेगा ?
उत्तर:
प्रश्न 4.
SO2Cl2 को अपनी प्रारम्भिक मात्रा से आधी मात्रा में वियोजित होने में 60 min का समय लगता है। यदि अभिक्रिया प्रथम कोटि की हो तो वेग स्थिरांक की गणना कीजिए।
उत्तर:
प्रश्न 5.
ताप का वेग स्थिरांक पर क्या प्रभाव होगा ?
उत्तर:
किसी अभिक्रिया का ताप 10°C बढ़ाने पर वेग स्थिरांक में लगभग दोगुनी वृद्धि होती है। वेग स्थिरांक की ताप पर निर्भरता आर्मेनियस समीकरण की सहायता से दे सकते हैं –
Ae-Ea/RT
यहाँ A = आवृति गुणक या पूर्व चरघातांकी गुणक है।
Ea = सक्रियण ऊर्जा
R = गैस नियतांक
T = ताप
प्रश्न 6.
परम ताप 298 K में 10 K की वृद्धि होने पर रासायनिक अभिक्रिया का वेग दोगुना हो जाता है। इस अभिक्रिया के लिए Ea की गणना कीजिए।
उत्तर:
प्रश्न 7.
581K ताप पर अभिक्रिया 2Hl(g) → H2(g) + l2(g) के लिये सक्रियण ऊर्जा का मान 209.5 kJ mol-1 है। अणुओं के उस अंश की गणना कीजिए जिसकी ऊर्जा सक्रियण ऊर्जा के बराबर अथवा इससे अधिक है।
उत्तर:
प्रश्न 8.
निम्नलिखित अभिक्रियाओं के वेग व्यंजकों से इनकी अभिक्रिया की कोटि तथा वेग स्थिरांकों की इकाइयाँ ज्ञात कीजिए –![]()
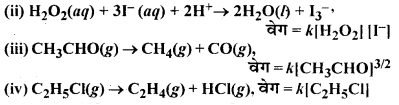
उत्तर:

प्रश्न 9.
अभिक्रिया 2A+ B → A2B के लिए वेग = k[A] [B]2, यहाँ k का मान 2.0 × 10-6 mol-2 L2 s-1 है। प्रारम्भिक वेग की गणना कीजिए, जब [A] = 0.1 mol L-1 एवं [B] = 0.2 mol L-1 हो तथा अभिक्रिया वेग की गणना कीजिए, जब [A] घटकर 0:06 mol L-1 रह जाये।
उत्तर:
प्रश्न 10.
प्लेटिनम सतह पर NH3 का अपघटन शून्य कोटि की अभिक्रिया है। N2 एवं H2 के उत्पादन की दर क्या होगी जब k का मान 2.5 × 10-4 mol L-1 s-1 हो ?
उत्तर:
प्रश्न 11.
रासायनिक अभिक्रिया के वेग पर प्रभाव डालने वाले कारकों का उल्लेख कीजिए।
उत्तर:
अभिक्रिया के वेग को प्रभावित करने वाले कारक निम्न हैं –
- सान्दण – अभिकारक की सान्द्रता बढ़ाने पर, अणुओं के आपस में टकराने की सम्भावना बढ़ जाती है फलस्वरूप अभिक्रिया का वेग बढ़ जाता है।
- ताप – ताप बढ़ाने पर अणुओं की गतिज ऊर्जा बढ़ जाती है जिसके कारण उनकी आपस में टक्कर भी बढ़ जाती है और अभिक्रिया का वेग भी बढ़ जाता है।
- दाब – दाब बढ़ाने पर गैसों के अणु पास-पास आ जाते हैं जिसके फलस्वरूप उनकी परस्पर टक्कर बढ़ जाती है फलतः अभिक्रिया का वेग भी बढ़ जाता है।
- अभिकारकों का पृष्ठ क्षेत्रफल – अभिकारकों का पृष्ठ क्षेत्रफल बढ़ाने पर भी अभिक्रिया का वेग बढ़ जाता है। उदाहरणार्थ, चूर्ण धातुओं में अभिक्रिया तीव्र गति से होती है।
- अभिकारकों की प्रकृति – यदि अभिकारक आयनिक है तो उस अभिक्रिया का वेग अनायनिक अभिक्रियाओं की तुलना में अधिक होता है।
प्रश्न 12.
किसी अभिकारक के लिए एक अभिक्रिया द्वितीय कोटि की है। अभिक्रिया का वेग कैसे प्रभावित होगा; यदि अभिकारक की सान्द्रता
(i) दोगुनी कर दी जाये
(ii) आधी कर दी जाये?
उत्तर:
प्रश्न 13.
जल में ऐस्टर के छद्म प्रथम कोटि के जल-अपघटन के अग्रलिखित आँकड़े प्राप्त हुए –
(i) 30 से 60 $ समय-अन्तराल में औसत वेग की गणना कीजिए।
(ii) एस्टर के जल-अपघटन के लिए छद्म प्रथम कोटि अभिक्रिया वेग स्थिरांक की गणना कीजिए।
उत्तर:

प्रश्न 14.
A और B के मध्य अभिक्रिया में A और B की विभिन्न प्रारम्भिक सान्दताओं के लिए प्रारम्भिक वेग (r0) नीचे दिये गये हैं –
उत्तर:
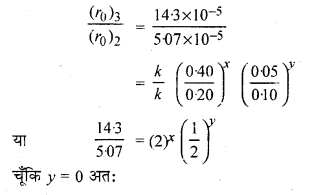

प्रश्न 15.
2A + B → C + D अभिक्रिया की बलगतिकी का अध्ययन करने पर निम्नलिखित परिणाम प्राप्त हुए। अभिक्रिया के लिए वेग नियम तथा वेग स्थिरांक ज्ञात कीजिए।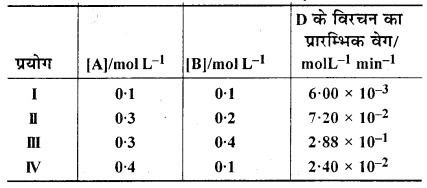
उत्तर:

प्रश्न 16.
A तथा B के मध्य अभिक्रिया A के प्रति प्रथम तथा B के प्रति शून्य कोटि की है। अग्रांकित तालिका में रिक्त स्थान भरिए –
उत्तर:
वेग समीकरण निम्नवत् होगा –
वेग = k[A]1 [B]0 = k[A]
प्रयोग के लिए : 2.0 × 10-2 mol L-1 min-1 = k (0.1M) या k = 0.2 min-1
प्रयोग II के लिए : 4.0 × 10-2 mol L-1 min-1 = 0.2 min-1 [A] या [A] = 0.2 mol L-1
प्रयोग III के लिए : वेग = 2.0 min-1 (0.4 mol L-1) = 0.08 mol L-1 min-1
प्रयोग IV के लिए: 2.0 × 10-2 mol L-1 min-1 = 0.2 min-1 [A] या [A] = 0.1 mol L-1
प्रश्न 17.
नीचे दी गई प्रथम कोटि की अभिक्रियाओं के वेग स्थिरांक से अर्द्ध-आयु की गणना कीजिए –
(i) 200 s-1
(ii) 2 min-1
(iii) 4 year-1.
उत्तर:
प्रथम कोटि की अभिक्रिया के लिए अर्द्ध-आयु,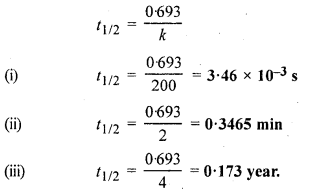
प्रश्न 18.
14C के रेडियोऐक्टिव क्षय की अर्द्ध-आयु 5730 वर्ष है। एक पुरातत्व कलाकृति की लकड़ी में, जीवित वृक्ष की लकड़ी की तुलना में 80% 14C की मात्रा है। नमूने की आयु का परिकलन कीजिए।
उत्तर:
रेडियोऐक्टिव क्षय एक प्रथम कोटि की अभिक्रिया है। प्रश्नानुसार, जीवित वृक्ष में 80% 14C है।
प्रश्न 19.
प्रथम कोटि की अभिक्रिया के लिए वेग स्थिरांक 60 s-1 है। अभिकारक को अपनी प्रारम्भिक सान्दता से [latex]frac { 1 }{ 16 } [/latex] वाँ भाग रह जाने में कितना समय लगेगा?
उत्तर:
प्रश्न 20.
नाभिकीय विस्फोट का 28.1 वर्ष अर्द्ध-आयु वाला एक उत्पाद 90Sr होता है। यदि कैल्सियम के स्थान पर 1 µg, 90Sr नवजात शिशु की अस्थियों में अवशोषित हो जाये और उपापचयन से ह्रास न हो तो इसकी 10 वर्ष एवं 60 वर्ष पश्चात् कितनी मात्रा रह जायेगी ?
उत्तर:


प्रश्न 21.
दर्शाइए कि प्रथम कोटि की अभिक्रिया में 99% अभिक्रिया पूर्ण होने में लगा समय 90% अभिक्रिया पूर्ण होने में लगने वाले समय से दोगुना होता है।
उत्तर:
99% अभिक्रिया पूर्ण होने में लगा समय,
प्रश्न 22.
एक प्रथम कोटि की अभिक्रिया में 30% वियोजन होने में 40 मिनट लगते हैं। t1/2 की गणना कीजिए।
उत्तर:
प्रश्न 23.
543 K ताप पर ऐजोआइसोप्रोपेन के हेक्सेन तथा नाइट्रोजन में विघटन के निम्नांकित आँकड़े प्राप्त हुए। वेग स्थिरांक की गणना कीजिए।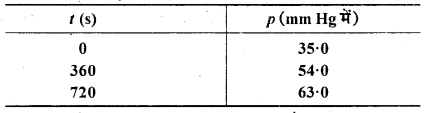
उत्तर:

प्रश्न 24.
स्थिर आयतन पर, SO2Cl2 के प्रथम कोटि के ताप अपघटन पर निम्नांकित आँकड़े प्राप्त हुए –
SO2Cl2 (g) → SO2(g) + Cl2 (g)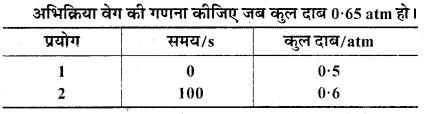
उत्तर:

प्रश्न 25.
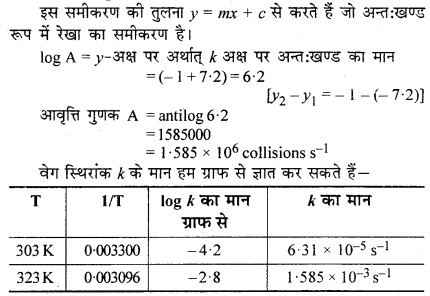
विभिन्न तापों पर N2O5 के अपघटन के लिए वेग स्थिरांक नीचे दिये गये हैं –
in k एवं [latex]frac { 1 }{ T } [/latex] के मध्य ग्राफ खींचिए तथा A एवं Ea की गणना कीजिए। 30°C तथा 50°C पर वेग स्थिरांक को प्रागुक्त कीजिए।
उत्तर:
log k तथा [latex]frac { 1 }{ T } [/latex] के मध्य ग्राफ खींचने के लिए हम निम्न सारणी बनाते हैं –
उपयुक्त मनोम पर आधारित ग्राफ निम्नलिखित चित्रों में प्रदर्शित है –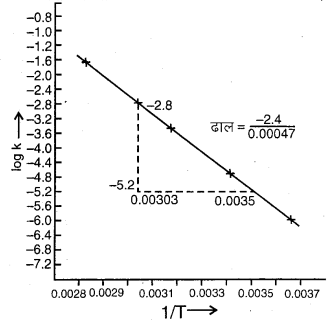

प्रश्न 26.
546 K ताप पर हाइड्रोकार्बन के अपघटन में वेग स्थिरांक 2.418 × 10-5 s-1 है। यदि सक्रियण ऊर्जा 179.9 kJ/mol हो तो पूर्व-घातांकी गुणन का मान क्या होगा ?
उत्तर:
प्रश्न 27.
किसी अभिक्रिया A → उत्पाद के लिए k = 2.0 × 10-2 s-1 है। यदि A की प्रारम्भिक सान्द्रता 1.0 mol L-1 हो तो 100 s के पश्चात् इसकी सान्दता क्या रह जायेगी ?
उत्तर:

प्रश्न 28.
अम्लीय माध्यम में सुक्रोस का ग्लूकोस एवं फ्रक्टोस में विघटन प्रथम कोटि की अभिक्रिया है। इस अभिक्रिया की अर्द्ध-आयु 3.0 घण्टे है। 8 घण्टे के बाद नमूने में सुक्रोस का कितना अंश बचेगा ?
उत्तर:

प्रश्न 29.
हाइड्रोकार्बन का विघटन निम्नांकित समीकरण के अनुसार होता है। सक्रियण ऊर्जा (Ea) की गणना कीजिए।
k = (4.5 × 1011 s-1) e-28000K/T
उत्तर:

प्रश्न 30.
H2O2 के प्रथम कोटि के विघटन को निम्नांकित समीकरण द्वारा लिख सकते हैं –
log k = 14.34 – 1.25 × 104 K/T
इस अभिक्रिया के लिए E, की गणना कीजिए। कितने ताप पर इस अभिक्रिया की अर्द्ध-आयु 256 मिनट होगी ?
उत्तर:

प्रश्न 31.
10°C ताप पर A के उत्पाद में विघटन के लिए k का मान 4.5 × 103 s-1 तथा सक्रियण ऊर्जा 60 kJ mol-1 है। किस ताप पर k का मान 1.5 × 104 s-1 होगा ?
उत्तर:
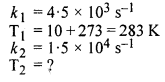

प्रश्न 32.
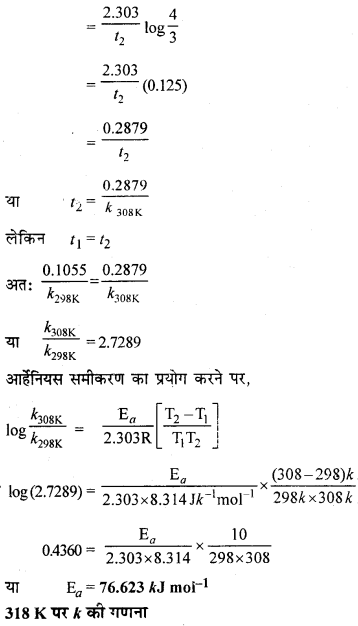
298 K ताप पर प्रथम कोटि की अभिक्रिया के 10% पूर्ण होने का समय 308 K ताप पर 25% अभिक्रिया पूर्ण होने में लगे समय के बराबर है। यदि A का मान 4 × 1010 sec-1 हो तो 318 K ताप पर k तथा Ea की गणना कीजिए।
उत्तर:
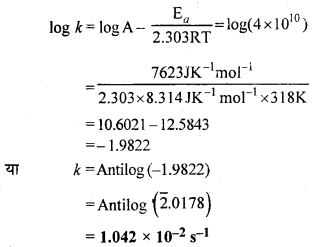
प्रश्न 33.
ताप में 293 K से 313 K तक वृद्धि करने पर किसी अभिक्रिया का वेग चार गुना हो जाता है। इस अभिक्रिया के लिए सक्रियण ऊर्जा की गणना यह मानते हुए कीजिए कि इसका मान ताप के साथ परिवर्तित नहीं होता।
उत्तर: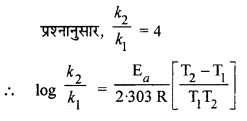
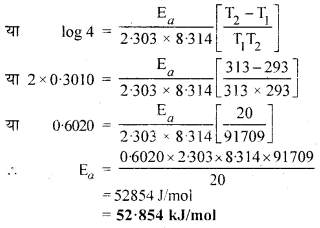
RBSE Class 12 Chemistry Chapter 4 रासायनिक बलगतिकी निबन्धात्मक प्रश्न
प्रश्न 1.
डाइमेथिल ईथर के अपघटन से CH4, H2 तथा CO बनते हैं। इस अभिक्रिया का वेग निम्नलिखित समीकरण द्वारा दिया जाता है –
वेग = k[CH3OCH3]3/2
अभिक्रिया के वेग को अनुगमन बन्द पात्र में बढ़ते दाब द्वारा किया जाता है, अतः वेग समीकरण को डाइमेथिल ईथर के आंशिक दाब के पद में भी दिया जा सकता है। अतः
वेग = k(pcH3OCH3)3/2
यदि दाब को bar में तथा समय को मिनट में मापा जाये तो अभिक्रिया के वेग एवं वेग स्थिरांक की इकाईयाँ क्या होंगी ?
उत्तर:
अभिक्रिया की कोटि = [latex]frac { 3 }{ 2 } [/latex]
अतः दाब के पदों में वेग स्थिरांक का नियतांक
= (bar)1-n min-1
= (bar)1-3/2 min-1
= bar-1/2 min-1.
वेग स्थिरांक की इकाई = (bar)-1/2 min-1
अभिक्रिया के वेग की इकाई = bar min-1
प्रश्न 2.
वेग स्थिरांक पर ताप का क्या प्रभाव पड़ता है ? ताप के इसे प्रभाव को मात्रात्मक रूप में कैसे प्रदर्शित कर सकते हैं ?
उत्तर:
किसी रासायनिक अभिक्रिया का ताप 10° (दस डिग्री) बढ़ाने पर वेग स्थिरांक के मान में दोगुनी वृद्धि होती है।
आर्मेनियस ने ताप एवं वेग स्थिरांक के मध्य में निम्न सम्बन्ध स्थापित किया –
Ae-Ea/RT
यहाँ A = आवृत्ति गुणक या आर्मेनियस गुणक या पूर्व चरघातांकी गुणक।
R = गैस नियतांक
Ea= सक्रियण ऊर्जा
T = ताप
k = वेग नियतांक।
प्रश्न 3.
एक अभिक्रिया A के प्रति प्रथम तथा B के प्रति द्वितीय कोटि की है।
(i) अवकलन वेग समीकरण लिखिए।
(ii) B की सान्द्रता तीन गुनी करने से वेग पर क्या प्रभाव पड़ेगा?
(iii) A तथा B दोनों की सान्द्रता दोगुनी करने से वेग पर क्या प्रभाव पड़ेगा ?
उत्तर:

प्रश्न 4.
गैस प्रावस्था में 318K पर N2O5 के अपघटन की [2N2O5 → 4NO2 + O2] अभिक्रिया के आँकड़े नीचे दिए गए हैं –
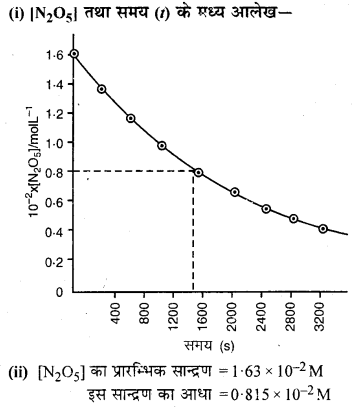
(i) [N2O5] एवं t के मध्य आलेख खींचिए।
(ii) अभिक्रिया के लिए अर्द्ध-आयु की गणना कीजिए।
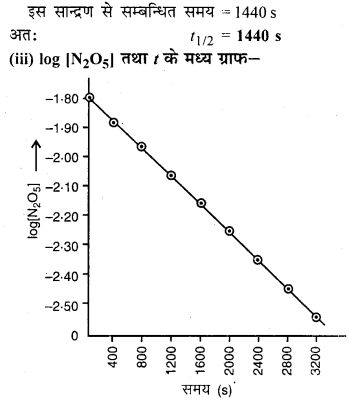
(iii) log [N2O5) एवं के मध्य ग्राफ खींचिए।
(iv) अभिक्रिया के लिए वेग नियम क्या है ?
(v) वेग स्थिरांक की गणना कीजिए।
(vi) k की सहायता से अर्द्ध-आयु की गणना कीजिए तथा इसकी तुलना (ii) से कीजिए।
उत्तर:


All Chapter RBSE Solutions For Class 12 Chemistry
—————————————————————————–
All Subject RBSE Solutions For Class 12
*************************************************
————————————————————
All Chapter RBSE Solutions For Class 12 Chemistry Hindi Medium
All Subject RBSE Solutions For Class 12 Hindi Medium
Remark:
हम उम्मीद रखते है कि यह RBSE Class 12 chemistry Solutions in Hindi आपकी स्टडी में उपयोगी साबित हुए होंगे | अगर आप लोगो को इससे रिलेटेड कोई भी किसी भी प्रकार का डॉउट हो तो कमेंट बॉक्स में कमेंट करके पूंछ सकते है |
यदि इन solutions से आपको हेल्प मिली हो तो आप इन्हे अपने Classmates & Friends के साथ शेयर कर सकते है और HindiLearning.in को सोशल मीडिया में शेयर कर सकते है, जिससे हमारा मोटिवेशन बढ़ेगा और हम आप लोगो के लिए ऐसे ही और मैटेरियल अपलोड कर पाएंगे |
आपके भविष्य के लिए शुभकामनाएं!!